题目内容
3.将浓度为0.1mol•L-1HF溶液加水不断稀释,下列各量始终保持增大的是( )| A. | [H+] | B. | Ka(HF) | C. | $\frac{[{F}^{-}]}{[{H}^{+}]}$ | D. | $\frac{[{H}^{+}]}{[HF]}$ |
分析 根据HF属于弱电解质,则在加水不断稀释时,电离程度增大,电离平衡保持向正反应方向移动,并注意温度不变时,电离平衡常数不变来解答.
解答 解:A、因HF为弱酸,则浓度为0.1mol•L-1HF溶液加水不断稀释,促进电离,平衡正向移动,电离程度增大,n(H+)增大,但c(H+)不断减小,故A错误;
B、因电离平衡常数只与温度有关,则Ka(HF)在稀释过程中不变,故B错误;
C、因稀释时一段时间电离产生等量的H+和F-,溶液的体积相同,则两种离子的浓度的比值不变,但随着稀释的不断进行,c(H+)不会超过10-7mol•L-1,c(F-)不断减小,则$\frac{[{F}^{-}]}{[{H}^{+}]}$的比值变小,故C错误;
D、因Ka(HF)=$\frac{c({F}^{-})×c({H}^{+})}{c(HF)}$,当HF溶液加水不断稀释,促进电离,c(F-)不断减小,Ka(HF)不变,则$\frac{[{H}^{+}]}{[HF]}$增大,故D正确;
故选:D.
点评 本题考查弱电解质的稀释,明确稀释中电离程度、离子浓度、Ka的变化即可解答,本题难点和易错点是不断稀释时c(H+)不会超过10-7mol•L-1.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.若丙醇中的氧原子为18O,它和乙酸反应生成的酯的相对分子质量为( )
| A. | 102 | B. | 104 | C. | 120 | D. | 122 |
14.设阿伏加德罗常数的数值为NA,下列叙述正确的是( )
| A. | 0.5 mol•L-1 NaOH溶液中Na+数为0.5NA | |
| B. | 标准状况下,22.4 L四氯化碳含有的分子数为NA | |
| C. | 常温常压下,1mol Na2O2与足量CO2反应,电子转移数为NA | |
| D. | 标准状况下,16 g氧气臭氧的混合气体所含原子数一定为2NA |
11. 利用如图装置测定中和热的实验步骤如下:
利用如图装置测定中和热的实验步骤如下:
①量取50mL 0.25mol•L-1硫酸倒入小烧杯中,测量温度;
②量取50mL 0.55mol•L-1NaOH溶液,测量温度;
③将NaOH溶液倒入小烧杯中,混合均匀后,测量混合液温度.请回答:
(1)从实验装置上看,图中尚缺少的一种玻璃用品是环形玻璃搅拌棒;
(2)NaOH溶液稍过量的原因确保硫酸被完全中和;
(3)加入NaOH溶液的正确操作是B(填字母).
A.沿玻璃棒缓慢加入 B.一次迅速加入 C.分三次加入
(4)使硫酸与NaOH溶液混合均匀的正确操作是用套在温度计上的环形玻璃搅拌棒轻轻地搅动;
(5)设溶液的密度均为1g/cm3,中和后溶液的比热容c=4.18J/(g•℃),请根据实验数据写出该反应的热化学方程式H2SO4(aq)+2NaOH(aq)=Na2SO4(aq)+2H2O△H=-113.68kJ/mol;
(6)上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)ac
a.实验装置保温、隔热效果差
b.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
c.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
(7)不能(填“能”或“不能”)用Ba(OH)2代替氢氧化钠溶液和稀硫酸反应;若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热量大于(填“小于”、“等于”或“大于”)57.3kJ.原因是浓硫酸稀释放热.
 利用如图装置测定中和热的实验步骤如下:
利用如图装置测定中和热的实验步骤如下:①量取50mL 0.25mol•L-1硫酸倒入小烧杯中,测量温度;
②量取50mL 0.55mol•L-1NaOH溶液,测量温度;
③将NaOH溶液倒入小烧杯中,混合均匀后,测量混合液温度.请回答:
(1)从实验装置上看,图中尚缺少的一种玻璃用品是环形玻璃搅拌棒;
(2)NaOH溶液稍过量的原因确保硫酸被完全中和;
(3)加入NaOH溶液的正确操作是B(填字母).
A.沿玻璃棒缓慢加入 B.一次迅速加入 C.分三次加入
(4)使硫酸与NaOH溶液混合均匀的正确操作是用套在温度计上的环形玻璃搅拌棒轻轻地搅动;
(5)设溶液的密度均为1g/cm3,中和后溶液的比热容c=4.18J/(g•℃),请根据实验数据写出该反应的热化学方程式H2SO4(aq)+2NaOH(aq)=Na2SO4(aq)+2H2O△H=-113.68kJ/mol;
| 温度 实验次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值(t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 25.0 | 25.2 | 28.5 | | |
| 2 | 24.9 | 25.1 | 28.3 | ||
| 3 | 25.5 | 26.5 | 31.8 | ||
| 4 | 25.6 | 25.4 | 29.0 | ||
a.实验装置保温、隔热效果差
b.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
c.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
(7)不能(填“能”或“不能”)用Ba(OH)2代替氢氧化钠溶液和稀硫酸反应;若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热量大于(填“小于”、“等于”或“大于”)57.3kJ.原因是浓硫酸稀释放热.
8.现有H+浓度相同的醋酸溶液和盐酸,分别用蒸馏水稀释至原体积的m倍和n倍,稀释后两溶液的H+浓度仍相等,则m和n的关系是( )
| A. | m>n | B. | m=n | C. | m<n | D. | 无法确定 |
15.下列反应的离子方程式书写正确的是( )
| A. | 用氢氧化钠溶液中和稀硝酸:H++OH-═H2O | |
| B. | 稀H2SO4与铁粉反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 氢氧化钡溶液与稀H2SO4反应:Ba2++SO42-═BaSO4↓ | |
| D. | 铜与硝酸银溶液的反应:Cu+Ag+═Cu2++Ag |
12.一定温度下,1molX和nmolY在体积为2L的密闭容器中发生如下反应:X(g)+Y(g)?Z(g)+W(s),10min后达到平衡,此时生成3amolZ下列说法正确的是( )
| A. | 用X表示此反应的反应速率是0.1(1-a)mol•(L•min)-1 | |
| B. | 当混合气体的质量不再发生变化时,说明反应达到平衡状态 | |
| C. | 向上述平衡体系中再充入1molX,v(正)增大,v(逆)减小,平衡正向移动 | |
| D. | 向平衡后的体系中加入1molW,平衡向逆反应方向移动 |
13.下列不是铁的氧化物的是( )
| A. | Fe3O4 | B. | Fe2O3 | C. | FeCl2 | D. | FeO |
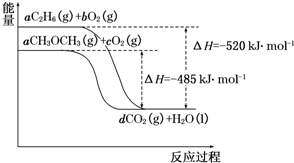 当今世界,能源的发展日益成为全世界、全人类共同关心的问题.如图是乙烷(C2H6)、二甲醚(CH3OCH3)燃烧过程的能量变化图.请回答下列问题:
当今世界,能源的发展日益成为全世界、全人类共同关心的问题.如图是乙烷(C2H6)、二甲醚(CH3OCH3)燃烧过程的能量变化图.请回答下列问题: