题目内容
一定温度下,一定体积的密闭容器中有如下平衡:H2(g)+I2(g)?2HI(g),已知H2和I2的起始浓度均为0.1mol?L-1时,达平衡时HI浓度为0.16mol?L-1.若H2和I2的起始浓度均变为0.2mol?L-1,则平衡时H2的浓度(mol?L-1)是( )
| A、0.16 | B、0.08 |
| C、0.04 | D、0.02 |
考点:化学平衡的计算
专题:化学平衡专题
分析:先根据题中所给信息,求出化学平衡常数,温度一定,化学平衡常数不变,再次利用平衡常数求出平衡式H2的浓度.
解答:
解:H2(g)+I2(g) 2HI(g)
2HI(g)
起始浓度0.10mol?L-1 0.10mol?L-1 0
反应浓度0.08mol?L-1 0.08mol?L-1.16mol?L-1
平衡浓度0.02mol?L-1 0.02mol?L-1 0.16mol?L-1
化学平衡常数K=
=
=64;
当H2和I2的起始浓度均变为0.20mol?L-1时,设则平衡时H2的浓度为x(mol?L-1),
则氢气的反应浓度为( 0.20-x)mol?L-1.
H2(g)+I2(g) 2HI(g)
2HI(g)
起始浓度 0.20mol?L-1 0.20mol?L-1 0
反应浓度 ( 0.20-x)mol?L-1 ( 0.20-x)mol?L-1 2(0.20-x)mol?L-1
平衡浓度 x x 2(0.20-x)mol?L-1
化学平衡常数K=
=64,
解得x=0.04 mol?L-1
故选:C.
 2HI(g)
2HI(g)起始浓度0.10mol?L-1 0.10mol?L-1 0
反应浓度0.08mol?L-1 0.08mol?L-1.16mol?L-1
平衡浓度0.02mol?L-1 0.02mol?L-1 0.16mol?L-1
化学平衡常数K=
| C 2(HI) |
| C(H 2)C(I 2) |
| 0.16 2 |
| 0.02×0.02 |
当H2和I2的起始浓度均变为0.20mol?L-1时,设则平衡时H2的浓度为x(mol?L-1),
则氢气的反应浓度为( 0.20-x)mol?L-1.
H2(g)+I2(g)
 2HI(g)
2HI(g)起始浓度 0.20mol?L-1 0.20mol?L-1 0
反应浓度 ( 0.20-x)mol?L-1 ( 0.20-x)mol?L-1 2(0.20-x)mol?L-1
平衡浓度 x x 2(0.20-x)mol?L-1
化学平衡常数K=
| 2(0.20-x)×2(0.20-x) |
| x×x |
解得x=0.04 mol?L-1
故选:C.
点评:温度一定,化学平衡常数不变是解决本题的关键.化学平衡常数K只受温度影响,与反应物或生成物的浓度变化无关.

练习册系列答案
相关题目
下列关于容量瓶及其使用方法的叙述,正确的是( )
①是配制一定物质的量浓度的溶液的专用仪器
②使用前要先检查容量瓶是否漏夜
③一定要用500mL容量瓶配制250mL溶液
④不能用容量瓶长期储存配置好的溶液
⑤容量瓶可以用来加热.
①是配制一定物质的量浓度的溶液的专用仪器
②使用前要先检查容量瓶是否漏夜
③一定要用500mL容量瓶配制250mL溶液
④不能用容量瓶长期储存配置好的溶液
⑤容量瓶可以用来加热.
| A、①③ | B、①②④ |
| C、①②④⑤ | D、①②③④ |
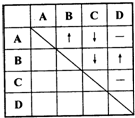 为了确定四瓶失去标签的五色溶液,它们分别是稀盐酸、稀硫酸、氢氧化钡和碳酸钠溶液,某同学采用了两两混合的方法.他能将四瓶溶液分别编号为A、B、C、D,然后各取少量在试管内两两混合,所观察到的现象如表中所示(“-”表示无明显现象;“↓”表示有沉淀生成:“↑”表示有气体生成.).
为了确定四瓶失去标签的五色溶液,它们分别是稀盐酸、稀硫酸、氢氧化钡和碳酸钠溶液,某同学采用了两两混合的方法.他能将四瓶溶液分别编号为A、B、C、D,然后各取少量在试管内两两混合,所观察到的现象如表中所示(“-”表示无明显现象;“↓”表示有沉淀生成:“↑”表示有气体生成.).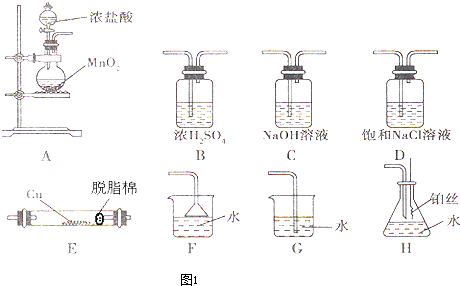
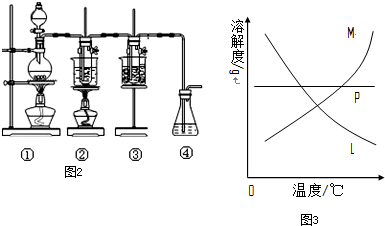
 工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为:2NH3 (g)+CO2 (g?CO(NH2)2 (l)+H2O (l),该反应的平衡常数和温度关系如下:
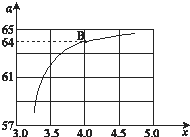
工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为:2NH3 (g)+CO2 (g?CO(NH2)2 (l)+H2O (l),该反应的平衡常数和温度关系如下: (1)在一定条件下,在水溶液中 1molCl-、ClOx-(x=1,2,3,4)的能量(kJ)的相对大小如图所示.
(1)在一定条件下,在水溶液中 1molCl-、ClOx-(x=1,2,3,4)的能量(kJ)的相对大小如图所示.