��Ŀ����
8����«����һ�ֿ�������ҩ��ϳ�����һ��·����ͼ��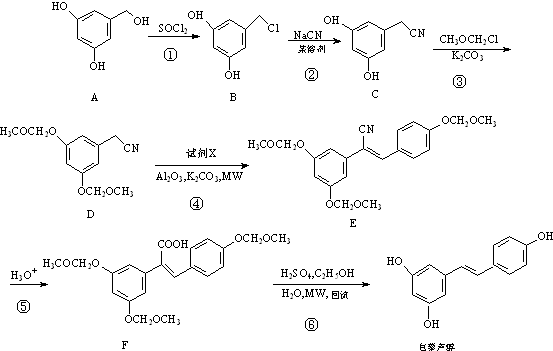
��1��������A���ڱ�¶�ڿ����л���ʣ���ԭ���Ƿ�������ױ������е�O2������
��2��������F�еĺ����������ҳ����Ե��������Ȼ���
��3����Ӧ���м���X�ķ���ʽΪC9H10O3��X�Ľṹ��ʽΪ
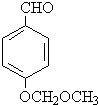 ��
����4���١��ܷ�Ӧ�У�����ȡ����Ӧ���Ǣ٢ڢۣ�
��5�����÷�Ӧ�۵�Ŀ���DZ������ǻ���
��6��D��һ��ͬ���칹����������������
�����ڦ������
����ʹ��ˮ��ɫ��������ʹFeCl3��Һ��ɫ
��������7�ֲ�ͬ��ѧ�������⣬�ұ����ϵ�һȡ����ֻ��һ�֣�
д���������������ĸ�ͬ���칹���һ�ֽṹ��ʽ
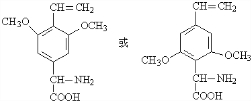 ��
����7����������֪ʶ����������Ϣ��д������ȩΪԭ���Ʊ�CH3CH�TC��CH3��COOH�ĺϳ�·������ͼ�����Լ����ã����ϳ�·������ͼʾ�����£�
CH3CH2Br$��_{��}^{NaOH��Һ}$CH3CH2OH$��_{Ũ���ᣬ��}^{CH_{3}COOH}$CH3COOCH2CH3
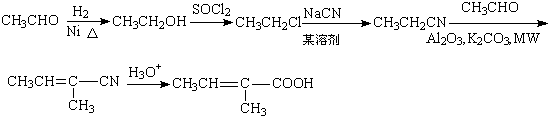 ��
��
���� ��1��A�к��з��ǻ����ױ�����������
��2����F�Ľṹ��ʽ��֪�����еĺ���������Ϊ�Ȼ����Ѽ��������Ȼ������ԣ�
��3����Ӧ���м����Լ�X�ķ���ʽΪC9H10O3���Ա�D��E�Ľṹ��X����ʽ��֪��D��X��ȥ1����ˮ�õ�E����D��-CN���ӵ��Ǽ���X��ȩ����ȥ1����ˮ�γ�̼̼˫�����õ�E��
��4����Ӧ����-Clȡ��-OH����������Ӧ����-CNȡ��-Cl����Ӧ���з��ǻ���Hԭ�ӱ�-OCH2OCH3ȡ������Ӧ�ܷ�����ˮ��Ӧͬʱ�γ�̼̼˫����������ȡ����Ӧ��
��5�����ǻ��ױ��������������ǻ���
��6��D��һ��ͬ���칹���������������������ڦ�-�����ᣬ���а������Ȼ����Ҷ�������ͬһ̼ԭ���ϣ�
����ʹ��ˮ��ɫ��������ʹFeCl3��Һ��ɫ���������ǻ������Ժ���̼̼˫������������7�ֲ�ͬ��ѧ�������⣬�ұ����ϵ�һȡ����ֻ��һ�֣������Ϻ���1��Hԭ�ӣ������й�����6�ֲ�ͬ��Hԭ�ӣ�
��7����ȩ�����������ӳɷ�Ӧ�����Ҵ����Ҵ�����ת����ϵ�Тٵķ�Ӧ�õ�CH3CH2Cl���ٽ�Ϸ�Ӧ�ڵõ�CH3CH2CN����Ϸ�Ӧ�ܿ�֪��CH3CH2CN����ȩ��Ӧ�õ�CH3CH=C��CH3��CN���ٸ��ݷ�Ӧ�ݣ�CH3CH=C��CH3��CN�ữ�õ�CH3CH=C��CH3��COOH��
��� �⣺��1����������ױ������е�O2���������ʣ�
�ʴ�Ϊ����������ױ������е�O2������
��2����F�Ľṹ��ʽ��֪�����еĺ���������Ϊ�Ȼ����Ѽ��������Ȼ������ԣ�
�ʴ�Ϊ���Ȼ���
��3����Ӧ���м����Լ�X�ķ���ʽΪC9H10O3���Ա�D��E�Ľṹ��X����ʽ��֪��D��X��ȥ1����ˮ�õ�E����D��-CN���ӵ��Ǽ���X��ȩ����ȥ1����ˮ�γ�̼̼˫�����õ�E������֪X�Ľṹ��ʽΪ�� ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��4���Ա����ʵĽṹ��֪����Ӧ����-Clȡ��-OH������������ȡ����Ӧ����Ӧ����-CNȡ��-Cl������ȡ����Ӧ����Ӧ���з��ǻ���Hԭ�ӱ�-OCH2OCH3ȡ��������ȡ����Ӧ����Ӧ�ܷ�����ˮ��Ӧͬʱ�γ�̼̼˫����������ȡ����Ӧ��
�ʴ�Ϊ���٢ڢۣ�
��5�����÷�Ӧ�۵�Ŀ���ǣ��������ǻ���
�ʴ�Ϊ���������ǻ���
��6��D��һ��ͬ���칹���������������������ڦ�-�����ᣬ���а������Ȼ����Ҷ�������ͬһ̼ԭ���ϣ�
����ʹ��ˮ��ɫ��������ʹFeCl3��Һ��ɫ���������ǻ������Ժ���̼̼˫������������7�ֲ�ͬ��ѧ�������⣬�ұ����ϵ�һȡ����ֻ��һ�֣������Ϻ���1��Hԭ�ӣ������й�����6�ֲ�ͬ��Hԭ�ӣ�����������ͬ���칹��Ϊ �ȣ�
�ȣ�
�ʴ�Ϊ�� ��
��
��7����ȩ�����������ӳɷ�Ӧ�����Ҵ����Ҵ�����ת����ϵ�Тٵķ�Ӧ�õ�CH3CH2Cl���ٽ�Ϸ�Ӧ�ڵõ�CH3CH2CN����Ϸ�Ӧ�ܿ�֪��CH3CH2CN����ȩ��Ӧ�õ�CH3CH=C��CH3��CN���ٸ��ݷ�Ӧ�ݣ�CH3CH=C��CH3��CN�ữ�õ�CH3CH=C��CH3��COOH���ϳ�·������ͼΪ�� ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���л���ĺϳɣ�ע������л���Ľ��н��з�������漰�����ŵĽṹ���л���Ӧ���͡���������ͬ���칹����д���ϳ�·����Ƶȣ���7����ע������ת����ϵ����������Ϣ���ϺõĿ���ѧ������Ϣ��ȡ��Ǩ�����ã��Ѷ��еȣ�

 ����5��2���ϵ�д�
����5��2���ϵ�д�
| A�� | �����ʱ����ϵ����ȴ����� 4 �� | |
| B�� | 1 mol �����ʺ� H2�ӳ������ҪH2�����ʵ���Ϊ 2 mol | |
| C�� | ��ʹ��ˮ��ɫ��1 mol �����ʺ���ˮ��ϣ�������� Br2�����ʵ���Ϊ 5 mol | |
| D�� | ������������ˮ����ʹ���Ը��������Һ��ɫ���ҷ������Ǽӳɷ�Ӧ |
| A�� | ����̫���ܡ���ϫ�ܡ��������磬���Ի�ȡ�����Դ | |
| B�� | ʳ���ͺ����Ͷ��������࣬����������ҵ���Ʒ��� | |
| C�� | ���ÿɽ���ġ��������ϡ�����һ���Է��У��ɷ�ֹ��ɫ��Ⱦ | |
| D�� | �ع�������������������������������˺�����Ӧ�����ӹ���������������� |
| A�� | ���ӽṹʾ��ͼ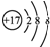 �����Ա�ʾ35Cl-��Ҳ���Ա�ʾ37Cl- �����Ա�ʾ35Cl-��Ҳ���Ա�ʾ37Cl- | |
| B�� | ����ʽ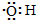 �����Ա�ʾ�ǻ���Ҳ���Ա�ʾ���������� �����Ա�ʾ�ǻ���Ҳ���Ա�ʾ���������� | |
| C�� | ����ģ�� �����Ա�ʾ������ӣ�Ҳ���Ա�ʾ���Ȼ�̼���� �����Ա�ʾ������ӣ�Ҳ���Ա�ʾ���Ȼ�̼���� | |
| D�� | �۱�ϩ�Ľṹ��ʽ��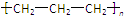 |
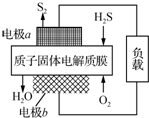 H2S������Դ������;��֮һ�ǻ����������õ�������Ӧԭ��Ϊ��2H2S��g��+O2��g���TS2��s��+2H2O��l����H=-632kJ•mol-1����ͼΪ����ĤH2Sȼ�ϵ�ص�ʾ��ͼ������˵����ȷ���ǣ�������
H2S������Դ������;��֮һ�ǻ����������õ�������Ӧԭ��Ϊ��2H2S��g��+O2��g���TS2��s��+2H2O��l����H=-632kJ•mol-1����ͼΪ����ĤH2Sȼ�ϵ�ص�ʾ��ͼ������˵����ȷ���ǣ�������| A�� | �缫aΪ��ص����� | |
| B�� | �缫b�Ϸ����ĵ缫��ӦΪ��O2+2H2O+4e-�T4OH- | |
| C�� | ��·��ÿ����4 mol���ӣ�����ڲ��ͷ�632 kJ���� | |
| D�� | ÿ34 g H2S���뷴Ӧ����2 mol H+������Ĥ���������� |
| A�� | 1molCl2�μӷ�Ӧת�Ƶ�������һ��Ϊ2NA | |
| B�� | ��16g18O2���10NA������ | |
| C�� | ��״���£�22.4L HF�к�2NA��ԭ�� | |
| D�� | 3mol����Fe��ȫת��ΪFe3O4��ʧȥ9NA������ |

���ֺ�����������ˮ�е��ܽ��������
| ���� | V2O5 | NH4VO3 | VOSO4 | ��VO2��2SO4 |
| �ܽ��� | ���� | ���� | ���� | ���� |
��1����Ӧ��������Һ�г�H+֮�����������VO2+��Al3+��
��2����Ӧ�ڼ�����˳��Ĺ�����Ҫ�ɷ���Al��OH��3��д��ѧʽ����
��3����Ӧ�ܵ����ӷ���ʽΪVO3-+NH4+=NH4VO3����
��4��25�桢101 kPaʱ��4Al��s��+3O2��g���T2Al2O3��s����H1=-a kJ/mol
4V��s��+5O2��g���T2V2O5��s����H2=-b kJ/mol
��V2O5�������ȷ�Ӧұ�����������Ȼ�ѧ����ʽ��10Al��s��+3V2O5��s��=5Al2O3��s��+6V��s����H=-$\frac{5a-3b}{2}$kJ/mol��
��5����Һ����أ���ͼ2��ʾ�����й�����Ӧ��������г�ǰ�����õ���и�Ĥֻ����H+ͨ������طŵ�ʱ�����ĵ缫��ӦʽΪV2+-e-=V3+����س��ʱ�����ĵ缫��Ӧʽ��VO2+-e-+H2O=VO2++2H+��
��6���������ữ��H2C2O4��Һ�ζ���VO2��2SO4��Һ���Բⶨ��Ӧ�ٺ���Һ�еĺ���������Ӧ�����ӷ���ʽΪ��2VO${\;}_{2}^{+}$+H2C2O4+2H+�T2VO2++2CO2��+2H2O��ȡ25.00mL0.1000 mol/L
H2C2O4����Һ����ƿ�У�����ָʾ����������Һʢ���ڵζ����У��ζ����յ�ʱ���Ĵ���Һ24.0mL���ɴ˿�֪���ã�VO2��2SO4��Һ�з��ĺ���Ϊ10.6g/L��
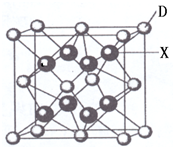 ��֪A��B��C��D��E�������ڱ���ǰ�����ڵ�Ԫ�أ����ǵĺ˵����A��B��C��D��E������A��B��C��ͬһ���ڵķǽ���Ԫ�أ�������DC 2�ľ���Ϊ���Ӿ��壬���������������ӵĸ�����Ϊ1��1��D�Ķ��������ӱ�C�ļ������Ӷ�һ�����Ӳ㣮AC 2Ϊ�Ǽ��Է��ӣ�B��C���⻯��ķе������ͬ����������Ԫ���⻯��ķе�ߣ�Eԭ������Ϊ26���ش��������⣺������ʱ��A��B��C��D��E������Ӧ��Ԫ�ط��ű�ʾ����
��֪A��B��C��D��E�������ڱ���ǰ�����ڵ�Ԫ�أ����ǵĺ˵����A��B��C��D��E������A��B��C��ͬһ���ڵķǽ���Ԫ�أ�������DC 2�ľ���Ϊ���Ӿ��壬���������������ӵĸ�����Ϊ1��1��D�Ķ��������ӱ�C�ļ������Ӷ�һ�����Ӳ㣮AC 2Ϊ�Ǽ��Է��ӣ�B��C���⻯��ķе������ͬ����������Ԫ���⻯��ķе�ߣ�Eԭ������Ϊ26���ش��������⣺������ʱ��A��B��C��D��E������Ӧ��Ԫ�ط��ű�ʾ����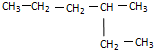 ��
��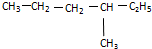 ��CS2
��CS2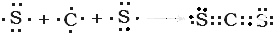 ��
��