题目内容
在KClO3+6HCl═3Cl2↑+KCl+3H2O中,有30mole-转移,生成的氯气在标准状况下的体积为( )
| A、22.4L |
| B、336.0L |
| C、403.2L |
| D、672.0L |
考点:氧化还原反应的计算
专题:氧化还原反应专题
分析:反应KClO3+6HCl(浓)=KCl+3Cl2+3H2O中,KClO3中Cl元素由+5价变为+0价,HCl中Cl元素由-1价变为0价,由方程式可知当有6molHCl参加反应时,有5mol被氧化,转移5mol电子,生成3molCl2,以此解答该题.
解答:
解:氧化还原反应K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O中,化合价升高元素Cl失电子,化合价降低元素Cr得电子,得失电子数目相等=反应中转移电子数=5,产生氯气3mol,此反应若转移了30mol的电子,产生氯气
mol,体积为:
mol×22.4L/mol=403.2L.
故选C.
| 90 |
| 5 |
| 90 |
| 5 |
故选C.
点评:本题考查氧化还原反应,侧重于学生的分析能力和计算能力的考查,为高考常见题型和高频考点,注意把握反应的特点,从元素化合价的角度解答该题,难度不大.

练习册系列答案
相关题目
锂电池是一种常用的电池,它广泛应用于心脏起搏器,一般可达十年之久,它的反应方程式为Li+MnO2═LiMnO2,下列有关它的说法错误的是( )
| A、它的负极是锂 |
| B、它的电解质溶液需用非水溶剂配制 |
| C、当有3.01×1023个电子转移时,正极消耗1mol |
| D、它是比容量(单位质量电极材料所能转换的电量)特别大的电池 |
下列有关实验装置进行的相应实验,能达到实验目的是( )
A、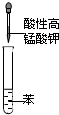 验证苯中是否有碳碳双键 |
B、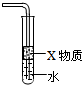 X若为苯,此装置可用于吸收氨气,防倒吸 |
C、 可除去HC1中含有的少量Cl2 |
D、 制备少量氧气 |
下列有关同分异构体数目的叙述中,错误的是( )
| A、甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有6种 |
| B、含有5个碳原子的饱和链烃,其一氯取代物共有8种 |
C、与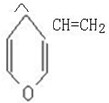 互为同分异构体的芳香族化合物有6种 互为同分异构体的芳香族化合物有6种 |
D、菲的结构简式为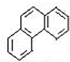 ,可有5种一硝基取代物 ,可有5种一硝基取代物 |
下列有关能量变化的说法中错误的是( )
| A、若反应物的总能量高于生成物的总能量,则该反应是吸热反应 |
| B、1mol石墨转化为金刚石,要吸收 1.895kJ的热能,则石墨比金刚石稳定 |
| C、化学变化中的能量变化主要由化学键的变化引起的 |
| D、化学变化必然伴随发生能量变化 |
下列化合物中,苯环上的氢原子被溴原子取代,所得一溴代物有三种同分异构体的是( )

| A、①③ | B、①④ | C、②③ | D、③④ |
含有非极性键的离子化合物是( )
| A、NaOH |
| B、Na2O2 |
| C、H2O2 |
| D、Cl2 |
下列有关化学反应中颜色变化描述错误的是( )
| A、石蕊试液中通入二氧化硫→红色 |
| B、内壁有油污的试管做银镜反应→黑色沉淀 |
| C、苯酚在空气中氧化→粉红色 |
| D、稀KI溶液中滴加少量FeCl3溶液→紫色 |
下列各组物质中,化学键类型完全相同的是( )
| A、HI和NaI |
| B、H2S和CO2 |
| C、H2O和NH4Cl |
| D、F2和NaBr |