题目内容
下列有关实验装置进行的相应实验,能达到实验目的是( )
A、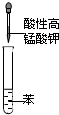 验证苯中是否有碳碳双键 |
B、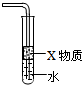 X若为苯,此装置可用于吸收氨气,防倒吸 |
C、 可除去HC1中含有的少量Cl2 |
D、 制备少量氧气 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.碳碳双键能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色;
B.有缓冲装置的能防止倒吸;
C.用饱和食盐水除去氯气中的氯化氢;
D.该装置反应的固体必须是块状的.
B.有缓冲装置的能防止倒吸;
C.用饱和食盐水除去氯气中的氯化氢;
D.该装置反应的固体必须是块状的.
解答:
解:A.碳碳双键能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,将酸性高锰酸钾溶液加入苯中,如果溶液褪色,说明苯中含有碳碳双键,否则不含碳碳双键,所以能实现实验目的,故A正确;
B.有缓冲装置的能防止倒吸,苯的目的小于水,所以苯浮在水面上,该装置没有缓冲装置,所以不能防止倒吸,则不能达到实验目的,故B错误;
C.氯化氢极易溶于水,氯气不易溶于饱和食盐水,所以用饱和食盐水除去氯气中的氯化氢而不是出去氯化氢中的氯气,所以不能达到实验目的,故C错误;
D.该装置反应的固体必须是块状的,过氧化钠是粉末状的,所以不能达到实验目的,故D错误;
故选A.
B.有缓冲装置的能防止倒吸,苯的目的小于水,所以苯浮在水面上,该装置没有缓冲装置,所以不能防止倒吸,则不能达到实验目的,故B错误;
C.氯化氢极易溶于水,氯气不易溶于饱和食盐水,所以用饱和食盐水除去氯气中的氯化氢而不是出去氯化氢中的氯气,所以不能达到实验目的,故C错误;
D.该装置反应的固体必须是块状的,过氧化钠是粉末状的,所以不能达到实验目的,故D错误;
故选A.
点评:本题考查了实验方案评价,明确实验原理是解本题关键,根据物质的性质结合实验装置来分析解答,知道防止尾气倒吸的方法有哪些,为常考查点,题目难度不大.

练习册系列答案
相关题目
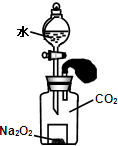 如图,集满CO2气体的广口瓶内,置有装一定量Na2O2(s)的小烧杯.向广口瓶内注入过量水(忽略体积变化),充分反应后恢复至原温度,气球体积几乎不变.此时小烧杯内的溶质是( )
如图,集满CO2气体的广口瓶内,置有装一定量Na2O2(s)的小烧杯.向广口瓶内注入过量水(忽略体积变化),充分反应后恢复至原温度,气球体积几乎不变.此时小烧杯内的溶质是( )| A、Na2CO3、NaOH |
| B、Na2CO3、Na2O2 |
| C、Na2CO3 |
| D、Na2CO3、NaHCO3 |
阿波罗宇宙飞船上使用的是氢-氧燃料电池,其电极总反应式为:2H2+O2═2H2O;电解质溶液为KOH溶液,下列叙述正确的是( )
| A、此电池能见到浅蓝色火焰 |
| B、H2为正极,O2为负极 |
| C、工作时电解液的pH不断增大 |
| D、电极反应为:正极 O2+2H2O+4e-=4OH- |
与亚硝酸乙酯(C2H5-ONO)互为同分异构体的是( )
①甘氨酸 ②乙酸铵 ③硝酸乙酯 ④硝基乙烷.
①甘氨酸 ②乙酸铵 ③硝酸乙酯 ④硝基乙烷.
| A、①② | B、①④ | C、②③ | D、③④ |
在NO2与H2O的反应中( )
| A、H2O是还原剂 |
| B、氧化剂与还原剂的质量比为2:1 |
| C、HNO3是氧化剂 |
| D、生成 1mol HNO3时,转移电子1mol |
根据表中信息,判断下列叙述中正确的是( )
| 序号 | 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 |
| ① | Cl2 | FeBr2 | / | Cl- | |
| ② | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
| ③ | KClO3 | 浓盐酸 | / | Cl2 |
| A、表中①组反应可能有一种或两种元素被氧化 |
| B、氧化性强弱比较:KClO3>Cl2>Fe3+>Br2 |
| C、表中②组反应的离子方程式是2MnO4-+3H2O2+6H+═2Mn2++4O2↑+6H2O |
| D、表中③组反应的还原产物是KCl,电子转移数目是6e- |
在KClO3+6HCl═3Cl2↑+KCl+3H2O中,有30mole-转移,生成的氯气在标准状况下的体积为( )
| A、22.4L |
| B、336.0L |
| C、403.2L |
| D、672.0L |
 在容积为2.0L的密闭容器内,物质D在T℃时发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,下列叙述错误的是( )
在容积为2.0L的密闭容器内,物质D在T℃时发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,下列叙述错误的是( )| A、从反应开始到第一次达到平衡时,A物质的平均反应速率为0.067mol/(L?min) | ||
B、根据图该反应的平衡常数表达式为k=
| ||
| C、若在第5分钟时升高温度,则该反应的正反应是吸热反应,反应的平衡常数增大,B的反应速率增大 | ||
| D、若在第7分钟时增加D的物质的量,A的物质的量变化情况符合b曲线 |
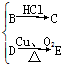 ,又知D不与Na2CO3溶液反应,C和E都不能发生银镜反应,则A可能的结构有( )
,又知D不与Na2CO3溶液反应,C和E都不能发生银镜反应,则A可能的结构有( )