题目内容
锂电池是一种常用的电池,它广泛应用于心脏起搏器,一般可达十年之久,它的反应方程式为Li+MnO2═LiMnO2,下列有关它的说法错误的是( )
| A、它的负极是锂 |
| B、它的电解质溶液需用非水溶剂配制 |
| C、当有3.01×1023个电子转移时,正极消耗1mol |
| D、它是比容量(单位质量电极材料所能转换的电量)特别大的电池 |
考点:化学电源新型电池
专题:电化学专题
分析:A、原电池的负极上是金属失电子的氧化反应;
B、根据金属锂可以和水之间发生化学反应来回答;
C、根据电极方程式和电子转移情况来回答;
D、根据锂电池是一种常用的电池,它广泛应用于心脏起搏器,一般可达十年之久来回答.
B、根据金属锂可以和水之间发生化学反应来回答;
C、根据电极方程式和电子转移情况来回答;
D、根据锂电池是一种常用的电池,它广泛应用于心脏起搏器,一般可达十年之久来回答.
解答:
解:A、根据电池反应方程式为Li+MnO2═LiMnO2,原电池的负极上是金属Li失电子的氧化反应,即Li是负极,故A正确;
B、由于金属锂可以和水之间发生化学反应,所以电池的电解质溶液需用非水溶剂配制,故B正确;
C、正极上的电极反应式为:MnO2+e-=MnO2-,当有3.01×1023个即0.5mol电子转移时,正极消耗0.5mol,故C错误;
D、根据锂电池的特点,知道它的比容量(单位质量电极材料所能转换的电量)特别大,故D正确.
故选C.
B、由于金属锂可以和水之间发生化学反应,所以电池的电解质溶液需用非水溶剂配制,故B正确;
C、正极上的电极反应式为:MnO2+e-=MnO2-,当有3.01×1023个即0.5mol电子转移时,正极消耗0.5mol,故C错误;
D、根据锂电池的特点,知道它的比容量(单位质量电极材料所能转换的电量)特别大,故D正确.
故选C.
点评:本题考查学生原电池的工作原理以及电极方程式的应用、电子守恒的有关计算等知识,注意知识的归纳和整理是关键,难度中等.

练习册系列答案
 学业测评一课一测系列答案
学业测评一课一测系列答案 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案
相关题目
 发展混合动力车是实施节能减排的重要措施之一.汽车上坡或加速时,电动机提供推动力,降低了汽油的消耗;在刹车和下坡时电动机处于充电状态以节省能耗.混合动力车的电动机目前一般使用的是镍氢电池,镍氢电池采用镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)电解液.镍氢电池充放电原理总反应式为:H2+2NiOOH═2Ni(OH)2.下列有关混合动力车的判断正确的是( )
发展混合动力车是实施节能减排的重要措施之一.汽车上坡或加速时,电动机提供推动力,降低了汽油的消耗;在刹车和下坡时电动机处于充电状态以节省能耗.混合动力车的电动机目前一般使用的是镍氢电池,镍氢电池采用镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)电解液.镍氢电池充放电原理总反应式为:H2+2NiOOH═2Ni(OH)2.下列有关混合动力车的判断正确的是( )| A、在上坡或加速时,乙电极周围溶液的pH将减小 |
| B、在上坡或加速时,溶液中的K+向甲电极迁移 |
| C、在刹车和下坡时,甲电极的电极反应式为:2H2O+2e-═H2↑+2OH- |
| D、在刹车和下坡时,乙电极增重 |
在一定条件下,向2L密闭容器中充入3mol X气和1mol Y气发生下列反应:2X(g)+Y(g)?3Z(g)+2W(g),在某一时刻达到化学平衡时,测出的下列各生成物浓度的数据中肯定错误的是( )
| A、c(Z)=0.75 mol/L |
| B、c(Z)=1.20 mol/L |
| C、c(W)=0.80 mol/L |
| D、c(W)=1.00 mol/L |
在30mL浓HNO3中,加入6.4g的Cu(Cu摩尔质量64g/mol),Cu完全溶解,收集到标准状况下气体2.24L,则下列说法中错误的是( )
| A、收集到的气体全部是NO2 |
| B、参加反应的HNO3为0.30mol |
| C、若HNO3无剩余,则原HNO3的浓度为10 mol?L-1 |
| D、被还原的HNO3与参加反应的HNO3的物质的量之比为1:3 |
化学科学需要借助化学专用语言来描述,下列化学用语不正确的是( )
A、Cl-的结构示意图: | ||
B、羟基的电子式: | ||
| C、HClO的结构式:H-Cl-O | ||
D、原子核内有10个中子的氧原子:
|
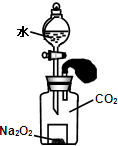 如图,集满CO2气体的广口瓶内,置有装一定量Na2O2(s)的小烧杯.向广口瓶内注入过量水(忽略体积变化),充分反应后恢复至原温度,气球体积几乎不变.此时小烧杯内的溶质是( )
如图,集满CO2气体的广口瓶内,置有装一定量Na2O2(s)的小烧杯.向广口瓶内注入过量水(忽略体积变化),充分反应后恢复至原温度,气球体积几乎不变.此时小烧杯内的溶质是( )| A、Na2CO3、NaOH |
| B、Na2CO3、Na2O2 |
| C、Na2CO3 |
| D、Na2CO3、NaHCO3 |
阿波罗宇宙飞船上使用的是氢-氧燃料电池,其电极总反应式为:2H2+O2═2H2O;电解质溶液为KOH溶液,下列叙述正确的是( )
| A、此电池能见到浅蓝色火焰 |
| B、H2为正极,O2为负极 |
| C、工作时电解液的pH不断增大 |
| D、电极反应为:正极 O2+2H2O+4e-=4OH- |
在KClO3+6HCl═3Cl2↑+KCl+3H2O中,有30mole-转移,生成的氯气在标准状况下的体积为( )
| A、22.4L |
| B、336.0L |
| C、403.2L |
| D、672.0L |
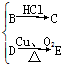 ,又知D不与Na2CO3溶液反应,C和E都不能发生银镜反应,则A可能的结构有( )
,又知D不与Na2CO3溶液反应,C和E都不能发生银镜反应,则A可能的结构有( )