题目内容
含有非极性键的离子化合物是( )
| A、NaOH |
| B、Na2O2 |
| C、H2O2 |
| D、Cl2 |
考点:离子化合物的结构特征与性质,极性键和非极性键
专题:化学键与晶体结构
分析:一般来说,活泼金属和活泼非金属元素之间易形成离子键,同种非金属元素之间易形成非极性共价键,不同非金属元素之间易形成极性共价键,含有离子键的化合物是离子化合物,离子化合物中可能含有共价键.
解答:
解:A.NaOH中钠离子和氢氧根离子之间存在离子键、O原子和H原子之间存在极性共价键,故A错误;
B.过氧化钠中钠离子和过氧根离子之间存在离子键、O原子之间存在非极性共价键,故B正确;
C.双氧水分子中H原子和O原子之间存在极性共价键、O原子之间存在非极性共价键,故B错误;
D.氯气分子中只存在非极性共价键,为单质,故D错误;
故选B.
B.过氧化钠中钠离子和过氧根离子之间存在离子键、O原子之间存在非极性共价键,故B正确;
C.双氧水分子中H原子和O原子之间存在极性共价键、O原子之间存在非极性共价键,故B错误;
D.氯气分子中只存在非极性共价键,为单质,故D错误;
故选B.
点评:本题考查了化合物类型及化学键类型的判断,根据物质的构成微粒及微粒间的作用力来分析解答,过氧化钠中存在的化学键及其电子式的书写是考试热点,题目难度不大.

练习册系列答案
相关题目
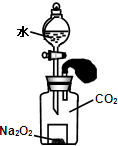 如图,集满CO2气体的广口瓶内,置有装一定量Na2O2(s)的小烧杯.向广口瓶内注入过量水(忽略体积变化),充分反应后恢复至原温度,气球体积几乎不变.此时小烧杯内的溶质是( )
如图,集满CO2气体的广口瓶内,置有装一定量Na2O2(s)的小烧杯.向广口瓶内注入过量水(忽略体积变化),充分反应后恢复至原温度,气球体积几乎不变.此时小烧杯内的溶质是( )| A、Na2CO3、NaOH |
| B、Na2CO3、Na2O2 |
| C、Na2CO3 |
| D、Na2CO3、NaHCO3 |
根据表中信息,判断下列叙述中正确的是( )
| 序号 | 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 |
| ① | Cl2 | FeBr2 | / | Cl- | |
| ② | KMnO4 | H2O2 | H2SO4 | O2 | Mn2+ |
| ③ | KClO3 | 浓盐酸 | / | Cl2 |
| A、表中①组反应可能有一种或两种元素被氧化 |
| B、氧化性强弱比较:KClO3>Cl2>Fe3+>Br2 |
| C、表中②组反应的离子方程式是2MnO4-+3H2O2+6H+═2Mn2++4O2↑+6H2O |
| D、表中③组反应的还原产物是KCl,电子转移数目是6e- |
在KClO3+6HCl═3Cl2↑+KCl+3H2O中,有30mole-转移,生成的氯气在标准状况下的体积为( )
| A、22.4L |
| B、336.0L |
| C、403.2L |
| D、672.0L |
某元素的原子具有三个电子层,关于其外围电子排布的正确说法是( )
| A、只有s电子 |
| B、只有p电子 |
| C、有s、p电子 |
| D、只有s电子或有s、p电子 |
关于CH4和 的叙述正确的是( )
的叙述正确的是( )
 的叙述正确的是( )
的叙述正确的是( )| A、均能用CnH2n+2组成通式来表示 |
| B、与所有烷烃互为同素异形体 |
| C、因为它们结构相似,所以它们的化学性质相似,物理性质相同 |
| D、通常情况下它们都是气态烷烃 |
在下列各组有机物中,既不属于同分异构体,又不属于同系物的一组物质是( )
| A、甲酸、乙酸、硬脂酸 |
| B、苯磺酸、苯甲酸、石炭酸 |
| C、2-丙醇、1-丙醇、甲乙醚 |
| D、丙醛、丙酮、丙烯醇(CH2=CH-CH2-OH) |
 在容积为2.0L的密闭容器内,物质D在T℃时发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,下列叙述错误的是( )
在容积为2.0L的密闭容器内,物质D在T℃时发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,下列叙述错误的是( )| A、从反应开始到第一次达到平衡时,A物质的平均反应速率为0.067mol/(L?min) | ||
B、根据图该反应的平衡常数表达式为k=
| ||
| C、若在第5分钟时升高温度,则该反应的正反应是吸热反应,反应的平衡常数增大,B的反应速率增大 | ||
| D、若在第7分钟时增加D的物质的量,A的物质的量变化情况符合b曲线 |
 海底热液研究处于当今科研的前沿,海底热液活动区域“黑烟囱”的 周围存在FeS、黄铜矿及锌矿等矿物.
海底热液研究处于当今科研的前沿,海底热液活动区域“黑烟囱”的 周围存在FeS、黄铜矿及锌矿等矿物.