题目内容
17.已知乙酸和乙酸乙酯的混合物中含H质量分数为7.8%,则其中含氧质量分数是( )| A. | 45.4% | B. | 49.8% | C. | 51.4% | D. | 15.6% |
分析 乙酸乙酯为C4H8O2,乙酸为C2H4O2,各分子中碳原子与氢原子数目之比为1:2,故混合物中碳元素与氢元素的质量之比为12:2=6:1,根据氢元素的质量分数计算混合物中碳元素质量分数,进而计算氧元素质量分数.
解答 解:乙酸乙酯为C4H8O2,乙酸为C2H4O2,各分子中碳原子与氢原子数目之比为1:2,故混合物中碳元素与氢元素的质量之比为12:2=6:1,混合物中氢元素的质量分数为7.8%,则混合物中碳元素的质量分数为7.8%×6=46.8%,故混合物中氧元素质量分数=1-7.8%-46.8%=45.4%,
故选A.
点评 本题考查混合物中元素的质量分数的计算,关键是根据各成分的化学式得出C、H的固定组成,学生应学会利用定组成的方法来解答混合物中元素的质量分数计算.

练习册系列答案
相关题目
7.下列有关物质用途的说法中,错误的是( )
| A. | 氯气可用于制漂白粉 | B. | 液氨可用作制冷剂 | ||
| C. | 活性炭可以去除冰箱中的异味 | D. | 二氧化硅可做半导体材料 |
8.科学家将液态的金属镓(Ga)充入碳纳米管中,发明出一种世界上最小的温度计-碳纳米管温度计.该温度计通过电子显微镜进行读数,精确度较高,其测量范围在18℃~490℃.下列说法错误的是( )
| A. | 碳纳米管中的镓为液体 | |
| B. | 金属镓的体积在10℃~500℃之间随温度的变化比较均匀 | |
| C. | 碳纳米管的体积在10℃~500℃之间随温度的变化很小 | |
| D. | Al(OH)3、Ga(OH)3均是两性氧化物 |
5.苹果酸的结构简式如图所示,下列说法正确的是( )
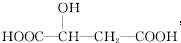
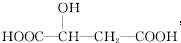
| A. | 苹果酸中能发生酯化反应的官能团有1种 | |
| B. | 1 mol苹果酸可与3 mol NaHCO3发生中和反应 | |
| C. | 1 mol苹果酸与足量金属 Na反应生成生成mol H2 | |
| D. | 1 mol苹果酸可以形成三元或四元环状内酯 |
12.下列关于化学式为[TiCl(H2O)5]Cl2•H2O的配合物的说法中正确的是( )
| A. | 配体是Cl-和H2O,配位数是9 | |
| B. | 中心离子是Ti3+,配离子是[TiCl(H2O)5]2+ | |
| C. | 内界和外界中的Cl-的数目比是 2:1 | |
| D. | 加入足量AgNO3溶液,所有Cl-均被完全沉淀 |
6.下列说法不正确的是( )
| A. | 金刚石跟石墨是同素异形体 | B. | 126C和146C是同位素 | ||
| C. | 不同的核素质子数可能相同 | D. | C2H4和C3H6一定是同系物 |
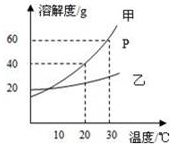 如图是甲、乙两种固体物质的溶解度曲线.据图回答:
如图是甲、乙两种固体物质的溶解度曲线.据图回答: