题目内容
7.下列有关物质用途的说法中,错误的是( )| A. | 氯气可用于制漂白粉 | B. | 液氨可用作制冷剂 | ||
| C. | 活性炭可以去除冰箱中的异味 | D. | 二氧化硅可做半导体材料 |
分析 A.氯气与氢氧化钙反应生成氯化钙和次氯酸钙和水;
B.液氨汽化吸收大量的热;
C.活性炭表面积大,具有吸附作用;
D.二氧化硅为绝缘体.
解答 解:A.工业用氯气与石灰乳反应制备漂白粉,故A正确;
B.液氨汽化吸收大量的热,可以做制冷剂,故B正确;
C.活性炭表面积大,具有吸附作用,可以去除冰箱中的异味,故C正确;
D.晶体硅导电性介于导体与绝缘体之间,可以做半导体,故D错误;
故选:D.
点评 本题考查了元素化合物知识,主要涉及物质的用途,明确相关物质的性质是解题关键,题目难度不大.

练习册系列答案
相关题目
8.在进行中和热的测定中,下列操作错误的是( )
| A. | 测量溶液的温度计要一直插在溶液中 | |
| B. | 应该向酸(碱)中慢慢滴加碱(酸) | |
| C. | 反应前需要用温度计测量酸(碱)温度 | |
| D. | 反应中酸或碱应适当过量 |
9.在反应MnO2+4HCl(浓)═MnCl2↑+Cl2↑+2H2O中,当有7.3g HCl被氧化时,生成Cl2的质量为( )
| A. | 14.2g | B. | 7.3g | C. | 3.65g | D. | 7.1g |
16.某厂平均每天产生约600m3废氨水(NH3 的浓度为153mg•L-1,密度为1g•cm-3.
(1)该废氨水中氨的物质的量浓度为9×10-3 mol•L-1.
(2)对废氨水进行加热蒸发得到NH3,使废氨水中的NH3的浓度降为17mg•L-1.忽略蒸发前后废氨水体积变化,则上述体积的废氨水蒸发出来的NH3的物质的量为4800mol.(以下计算结果均保留两位小数)
(3)蒸发得到的NH3可用于制备NO.4NH3+5O2→4NO+6H2O;(不考虑NO与氧气的反应),设空气中氧气的体积分数为0.20,氮气体积分数为0.80.
①为使NH3恰好完全氧化为NO,氨-空气混合物中氨的体积分数为89%.
②氨催化氧化制取NO同时会发生副反应:4NH3+3O2→2N2+6H2O.将1L NH3混合10L空气后通入反应器,反应完成后,测得混合气体中不含NH3,而O2和N2的物质的量之比为1:10,试求参加主反应的氨占原料氨的体积百分含量.
(4)废氨水可用于脱除烟气中的SO2.氨水吸收烟气中SO2经氧化后生成(NH4)2SO4和NH4HSO4混合物.现称取不同质量的混合物进行实验,结果如下:
试计算生成氨气的质量最大时样品的质量.
(1)该废氨水中氨的物质的量浓度为9×10-3 mol•L-1.
(2)对废氨水进行加热蒸发得到NH3,使废氨水中的NH3的浓度降为17mg•L-1.忽略蒸发前后废氨水体积变化,则上述体积的废氨水蒸发出来的NH3的物质的量为4800mol.(以下计算结果均保留两位小数)
(3)蒸发得到的NH3可用于制备NO.4NH3+5O2→4NO+6H2O;(不考虑NO与氧气的反应),设空气中氧气的体积分数为0.20,氮气体积分数为0.80.
①为使NH3恰好完全氧化为NO,氨-空气混合物中氨的体积分数为89%.
②氨催化氧化制取NO同时会发生副反应:4NH3+3O2→2N2+6H2O.将1L NH3混合10L空气后通入反应器,反应完成后,测得混合气体中不含NH3,而O2和N2的物质的量之比为1:10,试求参加主反应的氨占原料氨的体积百分含量.
(4)废氨水可用于脱除烟气中的SO2.氨水吸收烟气中SO2经氧化后生成(NH4)2SO4和NH4HSO4混合物.现称取不同质量的混合物进行实验,结果如下:
| NaOH 溶液体积/mL | 40.00 | 40.00 | 40.00 |
| 样品质量/g | 7.75 | 15.50 | 23.25 |
| 氨气质量/g | 1.87 | 1.87 | 1.7 |
17.已知乙酸和乙酸乙酯的混合物中含H质量分数为7.8%,则其中含氧质量分数是( )
| A. | 45.4% | B. | 49.8% | C. | 51.4% | D. | 15.6% |
 .
.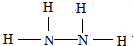 .
.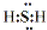 ;
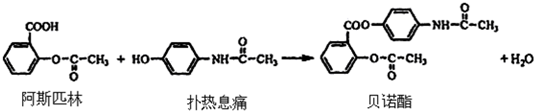
;
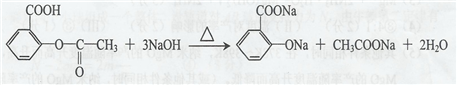 .
. .
.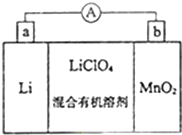 锂锰电池的体积小,性能优良,是常用的一次电池.该电池反应原理如图所示,其中电解质LiClO4溶于混合有机溶剂中,Li+ 通过电解质迁移入MnO2晶格中,生成LiMnO2.回答下列问题:
锂锰电池的体积小,性能优良,是常用的一次电池.该电池反应原理如图所示,其中电解质LiClO4溶于混合有机溶剂中,Li+ 通过电解质迁移入MnO2晶格中,生成LiMnO2.回答下列问题: