题目内容
19.下列化学实验事实及其解释不正确的是( )| A. | 钠保存在煤油中,是因为煤油不与钠发生反应,钠比煤油密度大,煤油可以使钠隔绝空气和水蒸气 | |
| B. | 用洁净的玻璃管向包有Na2O2的脱脂棉吹气,脱脂棉燃烧,说明CO2、H2O与Na2O2的反应是放热反应 | |
| C. | 滴有酚酞的NaHCO3溶液呈浅红色,微热后红色加深,是因为NaHCO3分解生成了Na2CO3. | |
| D. | 钠长期暴露在空气中的产物是Na2CO3,原因是钠与氧气生成的Na2O与水和二氧化碳反应 |
分析 A.性质决定物质的保存方法;
B.脱脂棉燃烧,可知反应放出热量;
C.滴有酚酞的NaHCO3溶液呈浅红色,与水解显碱性有关,且水解反应为吸热反应;
D.放置在空气中发生4Na+O2═2Na2O、Na2O+H2O=2NaOH、2NaOH+CO2=Na2CO3+H2O.
解答 解:A.因为煤油不与钠发生反应,钠比煤油密度大,煤油可以使钠隔绝空气和水蒸气,则钠保存在煤油中,故A正确;
B.用洁净的玻璃管向包有Na2O2的脱脂棉吹气,CO2、H2O与Na2O2反应生成氧气且放热,脱脂棉燃烧,说明CO2、H2O与Na2O2的反应是放热反应,故B正确;
C.滴有酚酞的NaHCO3溶液呈浅红色,微热后红色加深,是因为NaHCO3水解程度变大,碱性增强,不发生分解反应,故C错误;
D.钠放置在空气中和氧气反应生成氧化钠而变暗,反应方程式为4Na+O2═2Na2O,生成的氧化钠与水反应生成氢氧化钠,反应方程式为Na2O+H2O=2NaOH,生成的氢氧化钠在空气中与二氧化碳反应生成碳酸钠,反应方程式为2NaOH+CO2=Na2CO3+H2O,再形成碳酸钠晶体,最后风化得到Na2CO3,故D正确;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、试剂保存、反应中能量变化、盐类水解等为解答的关键,侧重分析与实验能力的考查,注意实验评价性分析,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.若NA表示阿伏加德罗常数值,下列说法正确的是( )
| A. | 2.4g Mg与Cl2完全反应,失去电子的数目为0.2NA | |
| B. | 标准状况下,NA个SO3分子所占的体积约为22.4L | |
| C. | 1mol Cl2与H2完全反应,转移的电子数目为NA | |
| D. | CO2的摩尔质量等于NA个CO2分子的质量 |
7.已知:SeO2+4KI+4HNO3═Se+2I2+4KNO3+2H2O,对于该氧化还原反应,下列说法错误的是( )
| A. | 硝酸在该反应中起酸性和氧化性作用 | |
| B. | 生成0.5molSe,转移电子数为2NA | |
| C. | I2是氧化产物 | |
| D. | 氧化剂和还原剂的物质的量之比为1:4 |
8.下列关于仪器使用的说法正确的是( )
| A. | 用四氯化碳萃取碘单质,静置,上层显示紫红色 | |
| B. | 坩埚需要垫石棉网加热 | |
| C. | 蒸馏时温度计水银球可以高于蒸馏烧瓶支管口 | |
| D. | 蒸发时用玻璃棒和向容量瓶移液时用玻璃棒用途不同 |
9.下列有关生活和生产中化学知识的描述错误的是( )
| A. | PVC保鲜膜属于链状聚合物,在加热时易熔化,能溶于氯仿 | |
| B. | 汽车尾气排放的NO2等气体是造成光化学污染的主要原因 | |
| C. | 点燃爆竹后,硫燃烧生成SO3 | |
| D. | 误食含有大量Cu2+的食物可以服用鲜牛奶解毒 |
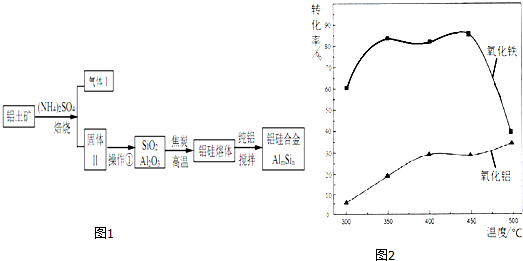
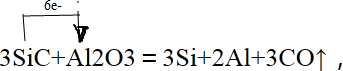 .
.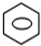 +HNO3(浓)$→_{55℃-60℃}^{浓硫酸}$
+HNO3(浓)$→_{55℃-60℃}^{浓硫酸}$ +H2O
+H2O )的一氯取代物共有种4,请写出其中任意两种的结构简式
)的一氯取代物共有种4,请写出其中任意两种的结构简式 或
或 、
、 或
或 .
.