题目内容
如右图所示,已知A的产量是一个国家石油化工水平的标志,D具有酸性.E是具有香味的不溶于水的液体.

(1)写出A分子的空间构型是: ,结构简式
(2)写出A→B的化学反应方程式: ,反应类型为: .
(3)写出B→C的化学反应方程式: ,反应类型为: .

(1)写出A分子的空间构型是:
(2)写出A→B的化学反应方程式:
(3)写出B→C的化学反应方程式:
考点:有机物的推断
专题:有机物的化学性质及推断
分析:A的产量通常用来衡量一个国家的石油化工水平,则A为乙烯,乙烯与水发生加成反应生成B为乙醇,乙醇氧化生成C,C氧化生成D,D具有酸性,故C为乙醛、D是乙酸,乙酸与乙醇生成具有果香味的物质E,E为乙酸乙酯,据此解答.
解答:
解:A的产量通常用来衡量一个国家的石油化工水平,则A为乙烯,乙烯与水发生加成反应生成B为乙醇,乙醇氧化生成C,C氧化生成D,D具有酸性,故C为乙醛、D是乙酸,乙酸与乙醇生成具有果香味的物质E,E为乙酸乙酯,
(1)A分子为乙烯,其空间构型是:平面性,含有碳碳双键,结构简式为CH2=CH2,
故答案为:平面形;CH2=CH2;
(2)A→B是乙烯与水发生加成反应生成乙醇,反应方程式为:CH2=CH2+H2O
CH3CH2OH,
故答案为:CH2=CH2+H2O
CH3CH2OH,加成反应;
(3)B→C是乙醇催化氧化生成乙醛,反应方程式为:2CH3CH2OH+O2
2CH3CHO+2H2O,
故答案为:2CH3CH2OH+O2
2CH3CHO+2H2O,氧化反应.
(1)A分子为乙烯,其空间构型是:平面性,含有碳碳双键,结构简式为CH2=CH2,
故答案为:平面形;CH2=CH2;
(2)A→B是乙烯与水发生加成反应生成乙醇,反应方程式为:CH2=CH2+H2O
| 一定条件 |
故答案为:CH2=CH2+H2O
| 一定条件 |
(3)B→C是乙醇催化氧化生成乙醛,反应方程式为:2CH3CH2OH+O2
| Cu |
| △ |
故答案为:2CH3CH2OH+O2
| Cu |
| △ |
点评:本题考查有机物的推断,比较基础,涉及烯烃、醇、醛、羧酸、酯的性质与转化,注意基础知识的掌握.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
锂原子比镁原子少1个电子层,最外层电子数也比镁原子少1,在周期表中锂和镁的位置关系存在有“对角线”关系,“对角线”关系的元素性质存在相似性.下列关于锂的判断可能正确的是( )
| A、Li能在空气中燃烧 |
| B、Li2O熔点较低 |
| C、Li2CO3能溶于水 |
| D、LiOH受热不易分解 |
下列说法正确的是( )
| A、第ⅥA族元素从上到下,其氢化物的稳定性逐渐减弱 |
| B、L层电子数为奇数的所有元素都是非金属元素 |
| C、ⅦA族元素阴离子的还原性越强,元素的最高价氧化物对应水化物的酸性也越强 |
| D、同一主族的甲乙两种元素,甲的原子序数为a,则乙的原子序数可能为a+4 |
在相同温度下,可逆反应X(g)+Y(g)?2Z(g),在四个体积相等的密闭容器内按下列配比进行反应,达到平衡时,Y的含量最低的是( )
| A、a mol X+a mol Y |
| B、2a mol Z |
| C、a mol X+a mol Z |
| D、a mol Y+a mol Z |
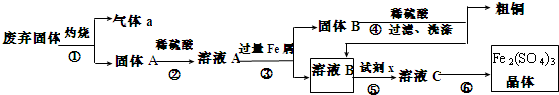
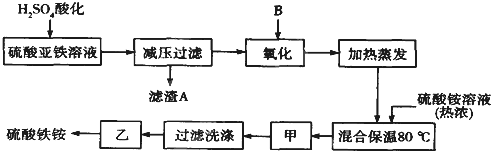
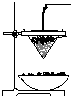 铁砂的主要成分是微粒状的磁性氧化铁、石英、石灰石等混合物.某化学兴趣小组从铁砂中分离出磁性氧化铁,并进行铝热反应实验.
铁砂的主要成分是微粒状的磁性氧化铁、石英、石灰石等混合物.某化学兴趣小组从铁砂中分离出磁性氧化铁,并进行铝热反应实验.