题目内容
下列说法正确的是( )
| A、1mol氧含有6.02×1023个微粒 |
| B、阿伏加德罗常数数值约等于6.02×1023 |
| C、钠的摩尔质量等于它的相对原子质量 |
| D、1mol任何气体所含的气体分子数目,不一定都相等 |
考点:阿伏加德罗常数,摩尔质量,气体摩尔体积
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.使用物质的量表示粒子时,必须指明具体的粒子名称;
B.根据阿伏伽德罗常数的近似值进行判断;
C.摩尔质量的单位为g/mol,相对原子量没有单位;
D.1mol任何气体都含有阿伏伽德罗常数个分子,含有的分子数一定相同.
B.根据阿伏伽德罗常数的近似值进行判断;
C.摩尔质量的单位为g/mol,相对原子量没有单位;
D.1mol任何气体都含有阿伏伽德罗常数个分子,含有的分子数一定相同.
解答:
解:A.1mol氧,没有指明是氧原子还是氧气分子,该表示方法不合理,故A错误;
B.1mol粒子中含有相应粒子的数目为阿伏伽德罗常数,其近似值为6.02×1023,故B正确;
C.钠的摩尔质量为23g/mol,钠的相对原子质量为23,二者的单位不同,故C错误;
D.1mol任何气体含有的分子数一定相同,含有的原子数可能不同,故D错误;
故选B.
B.1mol粒子中含有相应粒子的数目为阿伏伽德罗常数,其近似值为6.02×1023,故B正确;
C.钠的摩尔质量为23g/mol,钠的相对原子质量为23,二者的单位不同,故C错误;
D.1mol任何气体含有的分子数一定相同,含有的原子数可能不同,故D错误;
故选B.
点评:本题考查阿伏加德罗常数的有关计算和判断、摩尔质量与相对分子量的关系,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确摩尔质量与相对原子量的关系.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
硅及其化合物在材料领域中应用广泛,下列叙述错误的是( )
| A、石英(SiO2)是制造玻璃的重要原料之一 |
| B、石英砂可以用于制取高纯度的硅,硅是将太阳能转化为电能的常用材料 |
| C、Na2SiO3是制备硅胶和木材防火剂的原料 |
| D、晶体硅是制造光导纤维的材料 |
下面是一种三肽,它可以看作是3个氨基酸缩合而得到的产物
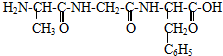
现有一个多肽分子,分子式为CXHYN12OD(X,Y,D为自然数)将它完全水解后只得到下列三种氨基酸
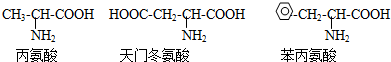
现将一个该多肽分子水解后,得到天门冬氨酸的分子个数为( )
现有一个多肽分子,分子式为CXHYN12OD(X,Y,D为自然数)将它完全水解后只得到下列三种氨基酸
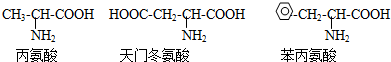
现将一个该多肽分子水解后,得到天门冬氨酸的分子个数为( )
| A、D-12 | ||
| B、D-13 | ||
C、
| ||
D、
|
下列说法中正确的是( )
①钠在空气中燃烧生成白色的固体氧化钠
②钠投入硫酸铜溶液中有红色粉末产生
③过氧化钠可在防毒面具中做供氧剂
④铁丝在氯气中燃烧产生大量红棕色的烟
⑤氢气在氯气中燃烧能产生大量的白烟.
①钠在空气中燃烧生成白色的固体氧化钠
②钠投入硫酸铜溶液中有红色粉末产生
③过氧化钠可在防毒面具中做供氧剂
④铁丝在氯气中燃烧产生大量红棕色的烟
⑤氢气在氯气中燃烧能产生大量的白烟.
| A、①② | B、②③ | C、③④ | D、④⑤ |
设NA为阿伏加德罗常数的数值,下列说法不正确的是( )
| A、常温下,1L pH=1的硫酸溶液中含有的H+为0.1NA |
| B、常温下,14g C2H4和C3H6的混合气体中含有2NA个氢原子 |
| C、2.3g Na和足量的O2完全反应,在常温和燃烧时,转移电子数均为0.1NA |
| D、1mol甲醇中含有C-H键的数目为4NA |