题目内容
如图是中学教材中元素周期表的一部分,其中标出A~Q 14种元素,试回答下列问题:

(1)在上表所列出的短周期元素中(填具体物质化学式)
①性质最不活泼的是 ;
②原子半径最小的是(除稀有气体元素) .
③形成的气态氢化物最稳定的是 ;
④最高价氧化物对应的水化物中酸性最强的是 ,单质氧化性最强的是 .
⑤形成的阴离子还原性最弱的是 ,简单阳离子半径最小的是 .
(2)用电子式表示A与C形成的化合物的形成过程 .
(3)F与K形成的高价化合物溶于水所克服的微粒间作用力为 .
(4)J在元素周期表中的位置是 ,B元素形成的单质的结构式为 ,K形成简单离子的结构示意图为 .
(5)设P的原子序数为Z,则F的原子序数为 (用Z表示),Q的原子序数为 (用Z表示).

(1)在上表所列出的短周期元素中(填具体物质化学式)
①性质最不活泼的是
②原子半径最小的是(除稀有气体元素)
③形成的气态氢化物最稳定的是
④最高价氧化物对应的水化物中酸性最强的是
⑤形成的阴离子还原性最弱的是
(2)用电子式表示A与C形成的化合物的形成过程
(3)F与K形成的高价化合物溶于水所克服的微粒间作用力为
(4)J在元素周期表中的位置是
(5)设P的原子序数为Z,则F的原子序数为
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:由元素在周期表中位置,可知A为碳、B为氮、C为O、D为氟、E为Na、F为Mg、G为Al、H为Si、I为磷、J为硫、K为Cl、L为Ar、P为Ba、Q为Pb.
(1)①稀有气体原子最外层为稳定结构,其化学性质最不活泼;
②同周期自左而右原子半径减小,同主族自上而下原子半径增大;
③非金属性越强,氢化物越稳定;
④最高价氧化物对应的水化物中酸性最强的是高氯酸;非金属性越强,其单质氧化性越强;
⑤非金属性越强,阴离子还原性越弱;电子层结构相同,核电荷数越大离子半径越小,电子层越多离子半径越大;
(2)A与C形成的高价化合物为CO2,分子中C原子与O原子之间形成2对共用电子对,用C原子、O原子电子式表示其形成;
(3)F与K形成的化合物为MgCl2,属于离子化合物,微粒键作用力为离子键;
(4)J位于第三周期16列,即位于第三周期ⅥA族;B元素形成的单质为N2,分子中N原子之间形成3对共用电子对;K形成简单离子为Cl-,离子核外有18个电子,有3个电子层,各层电子数为2、8、8;
(5)根据各周期容纳元素种数确定F、Q原子序数,F、P同主族,且处于过度元素之前,同主族相邻元素原子序数相差上一周期容纳元素种数,P、Q处于第六周期,分别处于2、14列,相差12列,其中该周期第3列容纳15种元素.
(1)①稀有气体原子最外层为稳定结构,其化学性质最不活泼;
②同周期自左而右原子半径减小,同主族自上而下原子半径增大;
③非金属性越强,氢化物越稳定;
④最高价氧化物对应的水化物中酸性最强的是高氯酸;非金属性越强,其单质氧化性越强;
⑤非金属性越强,阴离子还原性越弱;电子层结构相同,核电荷数越大离子半径越小,电子层越多离子半径越大;
(2)A与C形成的高价化合物为CO2,分子中C原子与O原子之间形成2对共用电子对,用C原子、O原子电子式表示其形成;
(3)F与K形成的化合物为MgCl2,属于离子化合物,微粒键作用力为离子键;
(4)J位于第三周期16列,即位于第三周期ⅥA族;B元素形成的单质为N2,分子中N原子之间形成3对共用电子对;K形成简单离子为Cl-,离子核外有18个电子,有3个电子层,各层电子数为2、8、8;
(5)根据各周期容纳元素种数确定F、Q原子序数,F、P同主族,且处于过度元素之前,同主族相邻元素原子序数相差上一周期容纳元素种数,P、Q处于第六周期,分别处于2、14列,相差12列,其中该周期第3列容纳15种元素.
解答:
解:由元素在周期表中位置,可知A为碳、B为氮、C为O、D为氟、E为Na、F为Mg、G为Al、H为Si、I为磷、J为硫、K为Cl、L为Ar、P为Ba、Q为Pb.
(1)①稀有气体原子最外层为稳定结构,故Ar化学性质最不活泼,故答案为:Ar;
②同周期自左而右原子半径减小,同主族自上而下原子半径增大,故上述元素中F原子半径最小,故答案为:F;
③同周期自左而右非金属性增强,同主族自上而下非金属性减弱,故上述元素中F的非金属性最强,非金属性越强,氢化物越稳定,故HF最稳定,故答案为:HF;
④最高价氧化物对应的水化物中酸性最强的是高氯酸,化学式为HClO4;上述元素中F的非金属性越强,其单质F2氧化性最强,故答案为:HClO4;F2;
⑤上述元素中F元素非金属性越强,故其阴离子F-的还原性最弱;电子层结构相同,核电荷数越大离子半径越小,电子层越多离子半径越大,故上述元素形成的阳离子中Al3+半径最小,故答案为:F-;Al3+;
(2)A与C形成的高价化合物为CO2,分子中C原子与O原子之间形成2对共用电子对,用C原子、O原子电子式表示其形成为: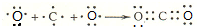 ,
,
故答案为: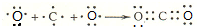 ;
;
(3)F与K形成的化合物为MgCl2,属于离子化合物,微粒键作用力为离子键,溶于水所克服的微粒间作用力为离子键,故答案为:离子键;
(4)J位于第三周期16列,即位于第三周期ⅥA族;B元素形成的单质为N2,分子中N原子之间形成3对共用电子对,其电子式为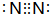 ,结构式为N≡N;K形成简单离子为Cl-,离子核外有18个电子,有3个电子层,各层电子数为2、8、8,离子结构示意图为:
,结构式为N≡N;K形成简单离子为Cl-,离子核外有18个电子,有3个电子层,各层电子数为2、8、8,离子结构示意图为: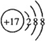 ,故答案为:第三周期ⅥA族;N≡N;
,故答案为:第三周期ⅥA族;N≡N; ;
;
(5)F、P同主族,且处于过度元素之前,同主族相邻元素原子序数相差上一周期容纳元素种数,设P的原子序数为Z,则F的原子序数为Z-8-18-18=Z-44,P、Q处于第六周期,分别处于2、14列,相差12列,其中该周期第3列容纳15种元素,故Q的原子序数=Z+15+(12-1)=Z+26,故答案为:Z-44;Z+26.
(1)①稀有气体原子最外层为稳定结构,故Ar化学性质最不活泼,故答案为:Ar;
②同周期自左而右原子半径减小,同主族自上而下原子半径增大,故上述元素中F原子半径最小,故答案为:F;
③同周期自左而右非金属性增强,同主族自上而下非金属性减弱,故上述元素中F的非金属性最强,非金属性越强,氢化物越稳定,故HF最稳定,故答案为:HF;
④最高价氧化物对应的水化物中酸性最强的是高氯酸,化学式为HClO4;上述元素中F的非金属性越强,其单质F2氧化性最强,故答案为:HClO4;F2;
⑤上述元素中F元素非金属性越强,故其阴离子F-的还原性最弱;电子层结构相同,核电荷数越大离子半径越小,电子层越多离子半径越大,故上述元素形成的阳离子中Al3+半径最小,故答案为:F-;Al3+;
(2)A与C形成的高价化合物为CO2,分子中C原子与O原子之间形成2对共用电子对,用C原子、O原子电子式表示其形成为:
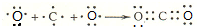 ,
,故答案为:
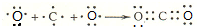 ;
;(3)F与K形成的化合物为MgCl2,属于离子化合物,微粒键作用力为离子键,溶于水所克服的微粒间作用力为离子键,故答案为:离子键;
(4)J位于第三周期16列,即位于第三周期ⅥA族;B元素形成的单质为N2,分子中N原子之间形成3对共用电子对,其电子式为
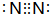 ,结构式为N≡N;K形成简单离子为Cl-,离子核外有18个电子,有3个电子层,各层电子数为2、8、8,离子结构示意图为:
,结构式为N≡N;K形成简单离子为Cl-,离子核外有18个电子,有3个电子层,各层电子数为2、8、8,离子结构示意图为: ,故答案为:第三周期ⅥA族;N≡N;
,故答案为:第三周期ⅥA族;N≡N; ;
;(5)F、P同主族,且处于过度元素之前,同主族相邻元素原子序数相差上一周期容纳元素种数,设P的原子序数为Z,则F的原子序数为Z-8-18-18=Z-44,P、Q处于第六周期,分别处于2、14列,相差12列,其中该周期第3列容纳15种元素,故Q的原子序数=Z+15+(12-1)=Z+26,故答案为:Z-44;Z+26.
点评:本题考查元素周期表与元素周期律,侧重对元素周期律与化学用语考查,注意理解掌握同族元素原子序数关系,掌握列与族的关系,难度中等.

练习册系列答案
相关题目
下列说法正确的是( )
| A、1mol氧含有6.02×1023个微粒 |
| B、阿伏加德罗常数数值约等于6.02×1023 |
| C、钠的摩尔质量等于它的相对原子质量 |
| D、1mol任何气体所含的气体分子数目,不一定都相等 |
设NA为阿伏加德罗常数,下列叙述中正确的是( )
| A、标准状况下,2.24L苯中约含有个NA碳原子 |
| B、标准状况下,22.4L H2中含中子数为2NA |
| C、1L 1mol/L醋酸溶液中离子总数为2NA |
| D、1mol Mg与足量O2或N2反应生成MgO或Mg3N2均失去2NA个电子 |
一氧化碳是一种用途相当广泛的化工基础原料,利用下列反应可以将粗镍转化为纯度达99.9%的高纯镍.
Ni(s)+4CO(g)?Ni(CO)4(g)在一密闭容器中,放入镍粉并充入一定量的CO气体,已知该反应的平衡常数如下表:下列说法正确的是( )
| 温度℃ | 25 | 80 | 230 |
| 平衡常数 | 5×10-4 | 2 | 1.9×10-5 |
| A、上述反应是熵增反应 |
| B、在80℃时,测得某时刻,Ni(CO)4、CO浓度均为0.5mol?L-1,则此时反应逆向进行 |
| C、25℃时,反应Ni(CO)4(g)?Ni(s)+4CO(g)的平衡常数是0.5 |
| D、恒温恒容,向达平衡的容器中再充入少量Ni(CO)4(g),达新平衡时,CO的百分含量将减小 |
下列实验中,颜色的变化与氧化还原反应无关的是( )
| A、SO2使酸性KMnO4溶液褪色 |
| B、Na2O2投入酚酞溶液中溶液先变红后褪色 |
| C、向FeSO4溶液中滴NaOH溶液,生成的沉淀由白色变成灰绿色,最后变成红褐色 |
| D、往紫色石蕊试液中通入氨气,溶液变蓝 |
 和
和 ;⑥
;⑥ 和
和 ;⑦
;⑦ 和
和  ;⑧CH3-CH2-CH=CH2 和CH2-CH=CH-CH2.
;⑧CH3-CH2-CH=CH2 和CH2-CH=CH-CH2.