题目内容
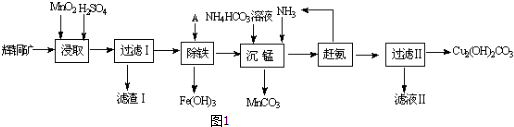
7.硒鼓回收料含硒约97%,其余为约3%的碲和微量的氯.从该回收料中回收硒的工艺流程如图所示(已知煅烧过程中,回收料中的硒、碲被氧化成SeO2和TeO2):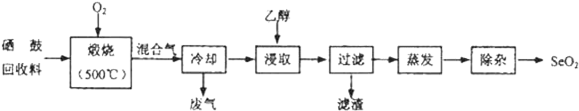
部分物质的物理性质如表:
| 物质 | 熔点 | 沸点 | 溶解度 |
| SeO2 | 340℃(315℃升华) | 684℃ | 易溶于水和乙醇 |
| TeO2 | 733℃(450℃升华) | 1260℃ | 微溶于水,不溶于乙醇 |
(1)Se与S是同族元素,比S多1个电子层,Se在元素周期表的位置为第四周期ⅥA族;H2Se的热稳定性比H2S的热稳定性弱(填“强”或“弱”).
(2)乙醇浸取后过滤所得滤渣的主要成分是TeO2.蒸发除去溶剂后,所得固体中仍含有少量TeO2杂质,除杂时适宜采用的方法是升华.
(3)SeO2易溶于水得到H2SeO3溶液,向溶液中通入HI气体后,再加入淀粉溶液,溶液变蓝色,同时生成Se沉淀,写出反应的化学方程式H2SeO3+4HI=Se↓+2I2+3H2O.
(4)已知H2SeO3的电离常数K1=3.5×10-3、K2=5.0×10-8,回答下列问题:
①Na2SeO3溶液呈碱性,原因是(用离子方程式表示)SeO32-+H2O?HSeO3-+OH-;
②在Na2SeO3溶液中,下列关系式正确的是C:
A.c(Na+)+c(H+)═c(SeO32-)+c(HSeO3-)+c(OH-)
B.2c(Na+)═c(SeO32-)+c(HSeO3-)+c(H2SeO3)
C.c(Na+)═2c(SeO32-)+2c(HSeO3-)+2c(H2SeO3)
D.c(OH-)═c(H+)+c(HSeO3-)+c(H2SeO3)
分析 硒鼓回收料含硒约97%,其余为约3%的碲和微量的氯,通入氧气煅烧过程中,回收料中的硒、碲被氧化成SeO2和TeO2,混合气体冷却得到物质加入乙醇浸取后过滤所得滤渣的主要成分TeO2 ,蒸发除去溶剂后,所得固体中仍含有少量TeO2杂质,利用升华分离除杂得到SeO2,
(1)Se与S是同族元素,比S多1个电子层,则Se核外含有4个电子层,最外层含有6个电子,据此判断其在周期表中的位置;根据非金属性强弱判断二者稳定性;
(2)煅烧后产物的主要成分为SeO2和TeO2,根据表中二者的性质解答;根据SeO2易升华分析;
(3)H2SeO3溶液与HI气体生成碘单质和Se沉淀;
(4)①H2SeO3是弱酸,水解呈碱性;
②A.c(SeO32-)带两个电荷;
BC.根据物料守恒解题;
D.根据质子守恒解题.
解答 解:(1)Se与S是同族元素,比S多1个电子层,则Se核外含有4个电子层,最外层含有6个电子,在元素周期表中位于第四周期、ⅥA族;同一主族中非金属性逐渐减弱,则非金属性S>Se,所以H2Se的热稳定性比H2S的热稳定性弱,
故答案为:第四周期ⅥA族;弱;
(2)煅烧后产物的主要成分为:和TeO2,由于TeO2微溶于水,不溶于乙醇,所以乙醇浸取后过滤所得滤渣的主要成分是TeO2;
由于SeO2易升华,则除去SeO2中少量Te02杂质,可通过升华的方法,故答案为:TeO2;升华;
(3)H2SeO3溶液与HI气体生成碘单质和Se沉淀,化学方程式:H2SeO3+4HI=Se↓+2I2+3H2O,故答案为:H2SeO3+4HI=Se↓+2I2+3H2O;
(4)①H2SeO3是弱酸,水解呈碱性,SeO32-+H2O?HSeO3-+OH-,故答案为:碱;SeO32-+H2O?HSeO3-+OH-;
②A.c(SeO32-)带两个电荷,应为c(Na+)+c(H+)=2c(SeO32-)+c(HSeO3-)+c(OH-),故A错误;
BC.钠原子个数为Se个数的二倍,c(Na+)=2c(SeO32-)+2c(HSeO3-)+2c(H2SeO3),故B错误、故C正确;
D.根据质子守恒可得:c(OH-)=c(HCO3-)+2c(H2CO3)+c(H+),故D错误.
故答案为:C.
点评 本题考查了物质制备方案的设计,题目难度中等,明确制备流程、发生反应原理为解答关键,涉及元素周期表应用、物质分离与除杂、化学方程式书写以及溶液中的离子浓度关系等知识,试题培养了学生的分析能力及化学实验能力.

| A. | 5.1 g | B. | 10.2 g | C. | 13.6 g | D. | 15.3 g |
①CS2+3Cl2$\frac{\underline{\;95-100℃\;}}{\;}$CCl4+S2Cl2;
②2S+Cl2$\frac{\underline{\;111-140℃\;}}{\;}$S2Cl2.
已知:S2Cl2易与水反应;S2Cl2+Cl2$\stackrel{△}{?}$2SCl2.
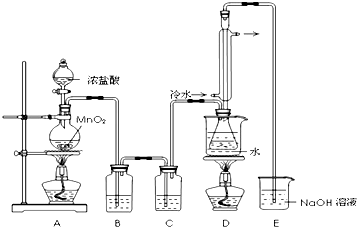
下表是几种物质的熔沸点,如图是反应装置图:
| 物质 | 沸点/℃ | 熔点/℃ |
| S | 445 | 113 |
| CS2 | 47 | -109 |
| CCl4 | 77 | -23 |
| S2Cl2 | 137 | -77 |
(2)若装置C更换成干燥管,则装置C中可选用的固体试剂是无水CaCl2(或固体P2O5).
(3)D装置中冷凝管的作用是冷凝、回流、导气;反应结束后,将D装置锥形瓶内的混合物中分离出产物的方法是蒸馏.
(4)S2Cl2与足量水反应有黄色沉淀生成,产生的无色气体能使品红溶液褪色,则该反应的化学方程式为2S2Cl2+2H2O═3S↓+SO2↑+4HCl↑.
(5)为了提高制得的产品S2Cl2的纯度,关键的操作是控制好温度和控制浓盐酸的滴速不能太快.
(6)上图尾部装置不够完善,改进措施是在D和E之间增加干燥装置,同时尾气吸收要防倒吸.
(7)若A中消耗了26.1g MnO2,得到10.8g产品,本实验的产率是80%.
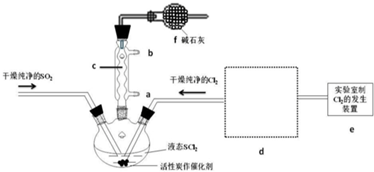
(1)仪器c的名称是球形冷凝管,装置f的作用是吸收逸出有毒的Cl2、SO2,防止空气中的水蒸气进入反应装置,防止SOCl2水解.
(2)SOCl2与水反应的化学方程式为SOCl2+H2O=SO2↑+2HCl↑.蒸干AlCl3溶液不能得到无水AlCl3,使SOCl2与AlCl3•6H2O混合加热,可得到无水AlCl3,试解释原因:AlCl3溶液易水解,AlCl3•6H2O与SOCl2混合加热,SOCl2与AlCl3•6H2O中的结晶水作用,生成无水AlCl3及SO2和HCl气体,SOCl2吸水,产物SO2和HCl抑制AlCl3水解.
(3)下列四种制备SO2的方案中最佳选择是丁.
| 方案 | 甲 | 乙 | 丙 | 丁 |
| 发生装置 | 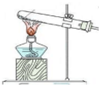 |  | 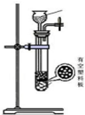 | 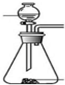 |
| 所选试剂 | NaHSO3固体 | 18.4mol/LH2SO4+Cu | 4mol/LHNO3+Na2SO3 | 70%H2SO4+K2SO3 |
(5)试验结束后,将三颈烧瓶中混合物分离开的实验操作是蒸馏;(已知SCl2的沸点为50℃)若反应中消耗的Cl2的体积为896ml(已转化为标准状况,SO2足量),最后得到纯净的SOCl24.76g,则SOCl2的产率为50% (保留三位有效数字).
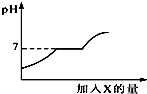 现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH随滴入X的量的变化关系如图所示.则X是( )
现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH随滴入X的量的变化关系如图所示.则X是( )| A. | 水 | B. | 澄清石灰水 | C. | 纯碱溶液 | D. | 稀盐酸 |