题目内容
下列化学用语正确的是( )
| A、Fe2(SO4)3与氨水反应:Fe3++3OH-=Fe(OH)3↓ |
| B、NaHCO3溶解于水电离:NaHCO3?Na++H++CO32- |
| C、NaHS的水解:HS-+H2O?H2S+OH- |
| D、Na2SO3的水解:SO32-+2H2O?H2SO3+2OH- |
考点:离子方程式的书写,电离方程式的书写,盐类水解的原理
专题:化学用语专题
分析:A.一水合氨属于弱碱,应保留化学式;
B.NaHCO3属于强电解质完全电离,碳酸氢根离子为弱酸的酸式根离子,不能拆;
C.NaHS的水解生成硫化氢和氢氧化钠;
D.亚硫酸根离子为多元弱酸根离子,分步水解.
B.NaHCO3属于强电解质完全电离,碳酸氢根离子为弱酸的酸式根离子,不能拆;
C.NaHS的水解生成硫化氢和氢氧化钠;
D.亚硫酸根离子为多元弱酸根离子,分步水解.
解答:
解:A.Fe2(SO4)3与氨水反应,离子方程式:Fe3++3NH3?H2O=Fe(OH)3↓+3NH4+,故A错误;
B.为NaHCO3溶解于水电离,离子方程式:NaHCO3=Na++HCO3-,故B错误;
C.NaHS的水解,离子方程:HS-+H2O?H2S+OH-,故C正确;
D.Na2SO3的水解,离子方程式:SO32-+H2O?HSO3-+OH-,故D错误;
故选:C.
B.为NaHCO3溶解于水电离,离子方程式:NaHCO3=Na++HCO3-,故B错误;
C.NaHS的水解,离子方程:HS-+H2O?H2S+OH-,故C正确;
D.Na2SO3的水解,离子方程式:SO32-+H2O?HSO3-+OH-,故D错误;
故选:C.
点评:本题考查了离子方程式的书写,明确反应的实质,盐类水解的规律及水解方程式书写的注意事项是解题关键,注意多元弱酸酸根离子分步水解.

练习册系列答案
相关题目
对于0.1mol/L的醋酸水溶液,下列说法中错误的是( )
| A、加入少量醋酸钠固体,则醋酸根离子浓度减少 |
| B、若加入少量冰醋酸,则氢离子浓度增大 |
| C、若加入少量的NaOH,则醋酸根离子浓度增大 |
| D、若加入少量的盐酸,则醋酸根离子浓度减少 |
下列说法正确的是( )
| A、1mol Na与足量O2反应,钠失去NA个电子 |
| B、目前加碘食盐中主要添加的是KI |
| C、Na2O与Na2O2都能和水反应生成碱,它们都是碱性氧化物 |
| D、Na2CO3溶液和NaHCO3溶液都能跟CaCl2溶液反应得到白色沉淀 |
NA为阿伏加德罗常数,下列叙述正确的是( )
A、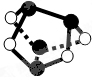 0.5mol雄黄(As4S4,已知As和N同主族,结构如图)含有NA个S-S键 |
| B、用惰性电极电解1 L浓度均为2 mol/L的AgNO3与Cu(NO3)2的混合溶液,当有0.2 NA个电子转移时,阴极析出6.4g金属 |
| C、1mol过氧化氢分子中共用电子对数为3NA |
| D、0.1mol Na2CO3?10H2O在晶体中或溶液中,含有的CO32-离子均小于0.1 NA |
下列有关实验的操作及描述不正确的是( )
| A、用托盘天平称取10.5g NaCl时应在右边托盘中放入10g砝码 |
| B、粗盐提纯时,为了加快过滤速率,可用玻璃棒搅拌过滤器中的液体 |
| C、分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D、测定溶液pH的操作:将pH试纸置于表面皿上,用玻璃棒蘸取溶液,点在pH试纸的中部,然后与标准比色卡对照 |
常温下,柠檬水溶液的PH是3,其中的C(OH-)是( )
| A、0.1mol/L |
| B、1.0×10-3 mol/L |
| C、1.0×10-11mol/L |
| D、1.0×10-7mol/L |
下列有关溶液中微粒浓度关系正确的是( )
| A、0.1 mol/L的NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
| B、等体积、等物质的量浓度的NaOH溶液与NaHCO3溶液混合后的溶液:c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3) |
| C、0.2 mol/L的某一元弱酸HA溶液和0.1 mol/LNaOH溶液等体积混合后的溶液:2c(OH-)+c(A-)=2c(H+)+c(HA) |
| D、常温下,NH4Cl和NH3?H2O的混合溶液[pH=7,c(Cl-)=0.1mol/L]中:c(Cl-)>c(NH4+)>c(OH-)=c(H+) |
下列各组物质互为同分异构体的是( )
| A、CH4与CH3CH3 | ||||
| B、正丁烷与异丁烷 | ||||
| C、O2与O3 | ||||
D、
|
下列有关物质的性质或应用的说法中正确的是( )
| A、浓硫酸具有吸水性,可用作干燥剂 |
| B、浓硝酸与铁不反应,可用铁桶贮存浓硝酸 |
| C、硅可作半导体材料,是光导纤维的主要成分 |
| D、SO2能使含有酚酞的NaOH溶液褪色,说明SO2具有漂白性 |