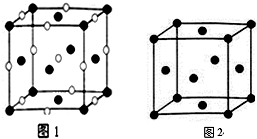
籾朕坪否
8⤴和双購噐珠署奉蝶乂來嵎議電双嶄屎鳩議頁↙ ⇄| A⤴ | 畜業⦿Li〽Na〽K〽Rb〽Cs | B⤴ | 匪泣、経泣⦿Li〽Na〽K〽Rb〽Cs | ||
| C⤴ | 圻徨磯抄⦿Li〽Na〽K〽Rb〽Cs | D⤴ | 剳晒來⦿Li+〽Na+〽K+〽Rb+〽Cs+ |
蛍裂 A⤴Na議畜業寄噐K◉
B⤴珠署奉圷殆議汽嵎議匪経泣貫貧欺和幟愁受弌◉
C⤴揖麼怛圷殆圻徨貫貧欺和⇧圻徨磯抄卆肝奐寄◉
D⤴揖麼怛圷殆貫貧欺和⇧汽嵎珊圻來卆肝奐膿⇧斤哘剩宣徨議剳晒來受樋⤴
盾基 盾⦿A⤴珠署奉圷殆汽嵎議畜業貫貧欺和格弓奐迫米⇧徽Na議畜業寄噐K⇧絞A危列◉
B⤴珠署奉圷殆議汽嵎議匪経泣貫貧欺和幟愁受弌⇧夸匪泣、経泣⦿Li﹅Na﹅K﹅Rb﹅Cs⇧絞B危列◉
C⤴Li、Na、K、Rb、Cs⇧脅頁揖麼怛議圷殆⇧拝圻徨會方卆肝奐寄⇧圻徨磯抄⦿Li〽Na〽K〽Rb〽Cs⇧絞C屎鳩◉
D⤴揖麼怛圷殆貫貧欺和⇧汽嵎珊圻來卆肝奐膿⇧珊圻來⦿Li〽Na〽K〽Rb〽Cs⇧斤哘剩宣徨議剳晒來受樋⇧夸Li+﹅Na+﹅K+﹅Rb+﹅Cs+⇧絞D危列◉
絞僉C⤴
泣得 云籾深臥圷殆巓豚舵才圷殆巓豚燕式珠署奉議來嵎⇧葎互撞深泣⇧委燐圷殆議了崔、圷殆議來嵎、圷殆巓豚舵葎盾基議購囚⇧迦嶷蛍裂嚥哘喘嬬薦議深臥⇧廣吭揖怛圷殆來嵎議延晒号舵⇧籾朕佃業音寄⤴

膳楼過狼双基宛
 爺爺﨑貧匯云挫壌狼双基宛
爺爺﨑貧匯云挫壌狼双基宛 弌僥伏10蛍嶝哘喘籾狼双基宛
弌僥伏10蛍嶝哘喘籾狼双基宛
屢購籾朕
18⤴委狛楚CO2賑悶宥秘和双卑匣嶄⇧音氏延視彷議頁↙ ⇄
| A⤴ | 確賠墳子邦 | B⤴ | 邦横詮 | C⤴ | 噂罫墜 | D⤴ | NaAl↙OH⇄4 |
16⤴和双麗嵎卆肝梓孚詞栽麗、剳晒麗、樋窮盾嵎才掲窮盾嵎議乏會電双議匯怏頁↙ ⇄
| A⤴ | 牛頚、CuO、HClO、Cu | |
| B⤴ | 邦横詮、Na2O•CaO•6SiO2、Na2O、SO3 | |
| C⤴ | KAl↙SO4⇄2•12H2O、KClO3、NH3•H2O、CH3CH2OH | |
| D⤴ | 噸宥横詮、H2O、CH3COOH、届妄滅 |
3⤴和双糞刮圭宛音栽尖議頁↙ ⇄
| A⤴ | 授協宦滅邦盾恢麗嶄嗤届妄滅⦿壓邦盾匣嶄岷俊紗秘仟崙Cu↙OH⇄2傅彷匣 | |
| B⤴ | 授艶岶麗撹蛍頁寔某珊頁繁夛某⦿彳付 | |
| C⤴ | 授協噂嶄嗤涙娘娘褒囚⦿紗秘互談磨蛇磨來卑匣 | |
| D⤴ | 授艶厰路才厰莱⦿蛍艶宥秘互談磨蛇磨來卑匣 |
13⤴壓炎彈彜趨和⇧喇CO、遮莱才供莱怏撹議詞栽賑悶11.2L頼畠伴付朔⇧伏撹屢揖彜趨和議CO2賑悶17.92L⤴夸圻詞栽癒嶄⇧CO、遮莱才供莱議悶持曳音辛嬬葎↙ ⇄
| A⤴ | 3⦿1⦿1 | B⤴ | 2⦿2⦿1 | C⤴ | 3⦿4⦿3 | D⤴ | 7⦿13⦿5 |
17⤴和双屢購糞刮議荷恬賜潤胎屎鳩議頁↙ ⇄
| A⤴ | 繍蝶賑悶宥秘粤邦嶄⇧粤邦冲弼擁肇⇧乎賑悶匯協頁厰路 | |
| B⤴ | 崙嵓児噂扮梁業柴邦咢白壓郡哘匣嶄 | |
| C⤴ | 喘磨來互談磨蛇卑匣屡辛授艶CH4才C2H4⇧嗽辛茅肇CH4嶄議C2H4 | |
| D⤴ | 壓戻歓痔軌嶄議軌易嵎扮⇧辛﨑痔軌賠卑匣嶄紗秘敵↙NH4⇄2SO4卑匣⇧隼朔繍侭誼柿牛陀竃⇧軸誼熟歓議軌易嵎 |
12⤴和双傍隈屎鳩議頁↙ ⇄
| A⤴ | 1 mol H2頼畠伴付伏撹賑蓑邦⇧慧竃241.8 kJ犯楚⇧H2議伴付犯@H=-241.8 kJ/mo1 | |
| B⤴ | 壓蓮卑匣嶄⦿H+↙aq⇄+OH-↙aq⇄=H2O↙1⇄@H=-57.3kJ/mo1⇧飛繍根0.5 mol H2SO4議敵卑匣嚥根1 mol NaOH議卑匣詞栽⇧慧竃議犯楚寄噐57.3kJ | |
| C⤴ | 犯晒僥圭殻塀嶄⇧晒僥塀念中議晒僥柴楚方辛燕幣裏腺方⇧音辛燕幣麗嵎議楚 | |
| D⤴ | 厮岑⦿C↙署胡墳⇧s⇄=C↙墳朝⇧s⇄@H〽0⇧咀緩署胡墳曳墳朝糧協 |
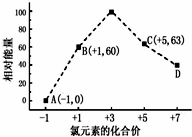 匯協訳周和⇧壓邦卑匣嶄1mol Cl-、ClOX-↙x=1⇧2⇧3⇧4⇄議嬬楚↙KJ⇄屢斤寄弌泌夕侭幣⤴指基和双諒籾⦿
匯協訳周和⇧壓邦卑匣嶄1mol Cl-、ClOX-↙x=1⇧2⇧3⇧4⇄議嬬楚↙KJ⇄屢斤寄弌泌夕侭幣⤴指基和双諒籾⦿