题目内容
3.下列实验方案不合理的是( )| A. | 鉴定蔗糖水解产物中有葡萄糖:在水解液中直接加入新制Cu(OH)2悬浊液 | |
| B. | 鉴别织物成分是真丝还是人造丝:灼烧 | |
| C. | 鉴定苯中有无碳碳双键:加入高锰酸钾酸性溶液 | |
| D. | 鉴别乙烯和乙烷:分别通入高锰酸钾酸性溶液 |
分析 A.检验葡萄糖应在碱性溶液中;
B.真丝的成分为蛋白质;
C.碳碳双键与高锰酸钾发生氧化反应,苯不能使高锰酸钾褪色;
D.乙烯能被高锰酸钾氧化,而乙烷不能.
解答 解:A.检验葡萄糖应在碱性溶液中,没有加碱至碱性,再加新制Cu(OH)2悬浊液,不能鉴定,故A错误;
B.真丝的成分为蛋白质,灼烧有烧焦羽毛的气体,则可鉴别,故B正确;
C.碳碳双键与高锰酸钾发生氧化反应,苯不能使高锰酸钾褪色,则高锰酸钾可鉴定苯中有无碳碳双键,故C正确;
D.乙烯能被高锰酸钾氧化,而乙烷不能,则高锰酸钾酸性溶液可鉴别乙烯和乙烷,故D正确;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,把握有机物的结构与性质、有机反应为解答的关键,侧重有机物鉴别及分析与应用能力的考查,注意有机反应的应用,题目难度中等.

练习册系列答案
相关题目
13.“春种一粒粟,秋收万颗子.”精选种子有利于提高农作物的产量,深圳市某农场工作人员配制了200kg某浓度的NaCl溶液选种,某学习小组取出731.25g NaCl溶液放置在一个大烧杯中,往烧杯中逐次加入AgNO3溶液测定其浓度,所得数据如图表所示.
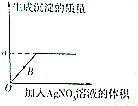 (1)生成沉淀的质量a=287.0g.
(1)生成沉淀的质量a=287.0g.
(2)在B点处,烧杯中溶液的溶质是NaNO3、NaCl(写化学式).
(3)该NaCl溶液的浓度是多少?(请写出详细的计算过程)
| 序号 | 1 | 2 | 3 | 4 | 5 |
| 每次加入AgNO溶液的体积/mL | 100 | 100 | 100 | 100 | 100 |
| 生成沉淀的质量/g | 71.75 | 143.5 | 215.25 | 287.0 | 287.0 |
 (1)生成沉淀的质量a=287.0g.
(1)生成沉淀的质量a=287.0g.(2)在B点处,烧杯中溶液的溶质是NaNO3、NaCl(写化学式).
(3)该NaCl溶液的浓度是多少?(请写出详细的计算过程)
8.下列关于碱金属某些性质的排列中正确的是( )
| A. | 密度:Li<Na<K<Rb<Cs | B. | 熔点、沸点:Li<Na<K<Rb<Cs | ||
| C. | 原子半径:Li<Na<K<Rb<Cs | D. | 氧化性:Li+<Na+<K+<Rb+<Cs+ |
15.在一定条件下,可以用如图(1)所示的硼化钒(VB2)-空气电池(工作时反应为:4VB2+11O2═4B2O3+2V2O5)为电源给图(2)所示装置通电,模拟有机物的电化学储氢.下列说法正确的是( )
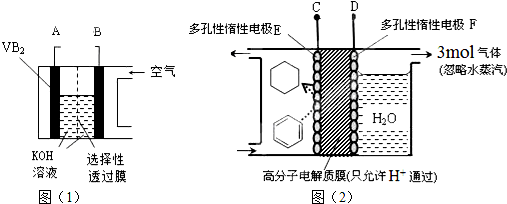

| A. | 整套装置工作时的连接为A连接D、B连接C | |
| B. | VB2极发生的电极反应为:2VB2+22OH--22e-═V2O5+2B2O3+11H2O | |
| C. | 电极F产生3mol气体时电极E得到的氧化产物为2mol | |
| D. | 储氢装置工作时,右侧电极区的pH值减小2×10-9 |
12.下列反应的离子方程式书写正确的是( )
| A. | 铝片放入氢氧化钠溶液中:Al+2OH-═AlO${\;}_{2}^{-}$+H2↑ | |
| B. | Na与水反应:Na+2H2O═Na++H2↑+2OH- | |
| C. | 向AlCl3溶液中加入过量NaOH溶液:Al3++3OH-═Al(OH)3↓ | |
| D. | AlCl3溶液中滴入过量的氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH${\;}_{4}^{+}$ |
 ④CH3COOH⑤HOCH2CHO ⑥CH3CH2CH2CH3⑦葡萄糖 ⑧蛋白质⑨淀粉
④CH3COOH⑤HOCH2CHO ⑥CH3CH2CH2CH3⑦葡萄糖 ⑧蛋白质⑨淀粉
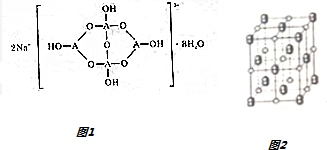

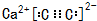 ,若晶胞的长、宽、高分别为520pm、520pm和690pm,则该晶体的密度为2.28g/cm3(精确至0.01)
,若晶胞的长、宽、高分别为520pm、520pm和690pm,则该晶体的密度为2.28g/cm3(精确至0.01)