题目内容
18.X、Y、Z、W均为短周期元素,他们在元素周期表的位置如图所示.若Y原子的最外层电子数与电子总数之比为3:4,下列说法正确的是( )| X | Y | |
| Z | W |
| A. | 原子半径:W>Z>Y>X | |
| B. | 最高价氧化物对应水化物的酸性:Z>W>X | |
| C. | 气态氢化物的稳定性:Z>W | |
| D. | W的单质能与水反应,生成一种具有漂白性的物质 |
分析 X、Y、Z、W均为短周期元素,若Y原子的最外层电子数与电子总数之比为3:4,则最外层电子数为6,电子总数为8,符合原子结构特点,则Y为O,结合位置可知X为N,Z为S,W为Cl,然后结合元素周期律及元素化合物知识来解答.
解答 解:X、Y、Z、W均为短周期元素,若Y原子的最外层电子数与电子总数之比为3:4,则最外层电子数为6,电子总数为8,符合原子结构特点,则Y为O,结合位置可知X为N,Z为S,W为Cl,
A.电子层越多,原子半径越大,同周期从左向右原子半径减小,则原子半径为Z>W>X>Y,故A错误;
B.非金属性W>Z>X,则最高价氧化物对应水化物的酸性为W>Z>X,故B错误;
C.非金属性W>Z,气态氢化物的稳定性为W>Z,故C错误;
D.W为Cl,其单质氯气与水反应生成HClO,具有漂白性,故D正确;
故选D.
点评 本题考查原子结构与元素周期律,为高频考点,把握原子结构推断元素Y为解答的关键,侧重分析与应用能力的考查,注意元素周期律及元素化合物知识运用,题目难度不大.

练习册系列答案
相关题目
8.下列分子中,既含有极性键又含有非极性键而且是非极性分子的是( )
| A. | CO2 | B. | CH4 | C. | C2H4 | D. | C2H5Cl |
13.下列说法不正确的是( )
| A. | ⅠA元素的电负性从上到下逐渐增大,而ⅦA元素的电负性从上到下逐渐减小 | |
| B. | 电负性的大小可以作为衡量元素的金属性和非金属性强弱的尺度 | |
| C. | 氢原子中只有一个电子,故氢原子只有一个原子轨道 | |
| D. | NaH的存在能支持可将氢元素放在ⅦA的观点 |
3.毒奶粉主要是奶粉中含有有毒的三聚氰胺(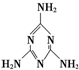 ).下列关于三聚氰胺分子的说法中正确的是( )
).下列关于三聚氰胺分子的说法中正确的是( )
 ).下列关于三聚氰胺分子的说法中正确的是( )
).下列关于三聚氰胺分子的说法中正确的是( )| A. | 所有氮原子均采取sp3杂化 | |
| B. | 一个三聚氰胺分子中共含有15个σ键 | |
| C. | 属于极性分子 | |
| D. | 三聚氰胺分子中同时含有极性键和非极性键 |
10.下列说法错误的是( )
| A. | 原子及其离子核外电子层数等于该元素所在的周期数 | |
| B. | 元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素 | |
| C. | 除氦外的稀有气体原子的最外层电子数都是8 | |
| D. | 质子数相同、电子数也相同的两种微粒,不可能是一种分子和一种离子 |
7.下列每组中各有三对物质,它们都能用分液漏斗分离的是( )
| A. | 乙酸乙酯和水,酒精和水,植物油和水 | |
| B. | 四氯化碳和水,溴苯和苯,硝基苯和水 | |
| C. | 甘油和水,乙酸和水,乙酸和乙醇 | |
| D. | 汽油和水,苯和水,己烷和水 |
8.下列对有机物结构或性质的描述中错误的是( )
| A. | 一定条件下,Cl2可与甲苯的苯环或侧链发生取代反应 | |
| B. | 1 mol乙烷和丙烯混合物完全燃烧生成3 molH2O | |
| C. | 用核磁共振氢谱不能鉴别1-丙醇和2-丙醇 | |
| D. | 邻二溴苯仅有一种空间结构,证明苯分子中不存在单双键交替的结构 |
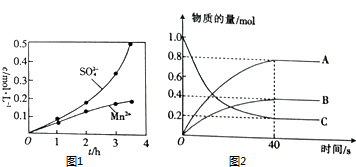 硫及其化合物在药物、造纸、炸药及石油加工等方面具有广泛应用.回答下列问题:
硫及其化合物在药物、造纸、炸药及石油加工等方面具有广泛应用.回答下列问题: