题目内容
下表各选项中,不能利用置换反应通过Y得到W的一组化合物是( )
| A | B | C | D | |
| Y | CO2 | Fe3O4 | CuCl2 | FeCl3 |
| W | MgO | Al2O3 | FeCl2 | CuCl2 |
| A、A | B、B | C、C | D、D |
考点:化学基本反应类型,常见金属元素的单质及其化合物的综合应用
专题:物质的性质和变化专题
分析:置换反应是一种单质和化合物反应生成另一种单质和化合物的反应,依据置换反应概念结合物质性质进行分析判断;
解答:
解:A.二氧化碳和镁反应生成碳和氧化镁,2Mg+CO2=C+2MgO,属于置换反应,故A不符合;
B.Fe3O4和Al反应生成氧化铝和铁,发生铝热反应,8Al+3Fe3O4=9Fe+4Al2O3,属于置换反应,故B不符合;
C、铁与与氯化铜反应生成氯化亚铁和铜,故C不符合;
D、氯化铁和铜反应只能生成氯化铁和氯化铜,故D符合;
故选:D;
B.Fe3O4和Al反应生成氧化铝和铁,发生铝热反应,8Al+3Fe3O4=9Fe+4Al2O3,属于置换反应,故B不符合;
C、铁与与氯化铜反应生成氯化亚铁和铜,故C不符合;
D、氯化铁和铜反应只能生成氯化铁和氯化铜,故D符合;
故选:D;
点评:本题考查了置换反应的概念应用,物质特征性质的分析判断,主要考查了镁、硅及其化合物、铁及其化合物性质的熟练掌握.

练习册系列答案
 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案
相关题目
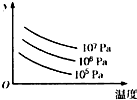 某密闭容器中,发生可逆反应L(s)+G(g)?3R(g)△H>0,如图表示温度、压强的变化对上述反应的影响.下列表述正确的是( )
某密闭容器中,发生可逆反应L(s)+G(g)?3R(g)△H>0,如图表示温度、压强的变化对上述反应的影响.下列表述正确的是( )| A、该反应达到平衡后加入适当的催化剂可提高G的转化率 |
| B、图中的y可能是达到平衡时G的转化率 |
| C、图中的y可能是平衡时混合气体中G的质量分数 |
| D、平衡后向容器中加入少量L,平衡右移,G的转化率增大 |
生活中处处有化学,请根据你所学过的化学知识,判断下列说法中错误的是( )
| A、抗酸药三硅酸镁的化学式为2MgO?3SiO2?nH2O |
| B、缺铁会引起骨质疏松症 |
| C、磺胺类药物是最早用于治疗全身性感染的人工合成抗菌药 |
| D、钡餐的主要成份为硫酸钡 |
下列叙述正确的是( )
| A、同温同压下,4Al(s)+3O2(g)═2Al2O3(s)在常温和点燃条件下的△H不同 | ||||||
| B、在某反应中,当反应物具有的总能量大于生成物具有的总能量时,该反应放热,△H>0 | ||||||
C、已知
| ||||||
| D、已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.4kJ?mol-1,则含20.0gNaOH的稀溶液与稀盐酸完全中和,放出28.7kJ的能量 |
下列反应常温时能自发进行,并既能用能量判据又能用熵判据解释的是( )
| A、HCl+NH3=NH4Cl |
| B、Ba(OH)2?8H2O+2 NH4Cl=BaCl2+NH3↑+10H2O |
| C、2KClO3=2KCl+3O2↑ |
| D、2Na2O2+2H2O=4NaOH+O2↑ |
已经Cu与稀硝酸的离子反应方程式如下(未配平):( )Cu+( )H++( )NO3-═( ) Cu2++( )NO↑+( )下列有关说法正确的是( )
| A、Cu是氧化剂,NO3-是还原剂 |
| B、还原剂与氧化剂的物质的量之比为3:2 |
| C、若生成1molNO,则转移2mol电子 |
| D、最后两空是4,H2O |
有Fe2+、NO3-、Fe3+、NH4+、H+、和H2O 六种微粒,分别属于同一氧化还原反应的反应物和生成物,且Fe2+Fe3+,下列说法中不正确的是( )
| A、氧化剂和还原剂物质的量之比为1:8 |
| B、该过程说明Fe(NO3)2溶液不宜加酸酸化 |
| C、若有1mol NO3- 发生氧化反应,则转移8mol电子 |
| D、若该反应HNO3参加,则HNO3表现氧化性和酸性 |
火箭发射的燃料有很多,偏二甲肼(C2H8N2)是一种高能燃料,燃烧产生巨大能量,可作为航天运载火箭的推动力.下列叙述中正确的是( )
| A、6.02×1023个偏二甲肼分子的质量为60g |
| B、偏二甲肼的摩尔质量为60g |
| C、1mol偏二甲肼的质量为60g/mol |
| D、6g偏二甲肼含有NA个偏二甲肼分子 |