题目内容
15.M的名称是乙烯雌酚,它是一种激素类药物,结构简式如图.下列叙述不正确的是( )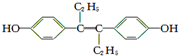
| A. | M的分子式为C18H20O2 | |
| B. | 1 mol M与饱和溴水混合,最多消耗5 mol Br2 | |
| C. | 1 mol M最多能与7 mol H2发生加成反应 | |
| D. | M与NaOH溶液或NaHCO3溶液均能反应 |
分析 该物质中含有酚羟基、苯环、碳碳双键,具有酚、苯、烯烃性质,能发生取代反应、氧化反应、加成反应、加聚反应等,据此分析解答.
解答 解:A.根据结构简式知,其分子式为C18H20O2,故A正确;
B.碳碳双键、酚羟基邻对位氢原子能和溴反应,则1 mol M与饱和溴水混合,最多消耗5 mol Br2,故B正确;
C.碳碳双键和苯环能和氢气在一定条件下发生加成反应,则1 mol M最多能与7 mol H2发生加成反应,故C正确;
D.酚羟基能和碳酸钠反应而不能和碳酸氢钠反应,酚羟基能和NaOH反应,故D错误;
故选D.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,侧重考查酚和烯烃性质,注意酚和溴发生取代反应位置,题目难度不大.

练习册系列答案
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案
相关题目
5.下列叙述中,正确的是( )
| A. | 两种粒子,若核外电子排布完全相同,则其化学性质相同 | |
| B. | 凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布 | |
| C. | 一种微粒与另一种微粒的质子数和电子数均相等,它们可能是一种离子和一种分子 | |
| D. | 不存在两种质子数和电子数均相同的阳离子和阴离子 |
6.20世纪80年代中期,科学家发现并证明碳还以新的单质形态C60存在.后来人们又相继得到了C70、C76、C84、C90、C94等另外一些球碳分子.90年代初,科学家又发现了管状碳分子和洋葱状碳分子.(如图):下列说法错误的是( )
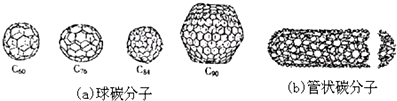

| A. | 金刚石和石墨的熔点肯定要比C60高 | |
| B. | 据估计C60熔点比金刚石和石墨要高 | |
| C. | 无论是球碳分子,还是管状碳分子、洋葱状碳分子,都应看作是碳的同素异形体 | |
| D. | C60的熔点低于C90 |
20.甲烷与氯气发生取代反应,生成的四种不同的氯代物中,分子结构为正四面体型的是( )
| A. | CH3Cl | B. | CH2Cl2 | C. | CHCl3 | D. | CCl4 |
7.下列能作为比较氧元素和氯元素的非金属性强弱的是( )
| A. | H2SO4的酸性比HClO3酸性强 | |
| B. | Fe在纯氧中燃烧生成Fe3O4,Fe在氯气中燃烧生成FeCl3 | |
| C. | 在HClO中,元素化合价氯为+1价,氧为-2价 | |
| D. | O2为无色无味气体,Cl2为黄绿色有刺激性气味的气体 |
4.下列说法中正确的是( )
| A. | 原子及其离子的核外电子层数等于该元素所在的周期数 | |
| B. | 元素周期表中从 IIIB 族到 IIB 族 10 个纵行的元素都是金属元素 | |
| C. | 第ⅠA 族元素的金属性比第ⅡA 族元素的金属性强 | |
| D. | 在周期表里,主族元素所在的族序数等于原子核外电子数 |
5.下列过程能同时生成两种盐的是( )
| A. | Na2O2投入水中 | B. | 铜片投入到FeCl3溶液中 | ||
| C. | NaHCO3溶液和NaOH溶液混合 | D. | 过量氨水加入到AlCl3溶液 |
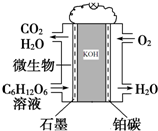 微生物燃料电池是利用微生物作为反应主体,将有机物的化学能转化为电能.如以葡萄糖溶液为例,其工作原理如图所示:
微生物燃料电池是利用微生物作为反应主体,将有机物的化学能转化为电能.如以葡萄糖溶液为例,其工作原理如图所示: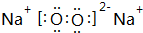 ,其中含有的化学键为离子键、共价键.
,其中含有的化学键为离子键、共价键.