题目内容
7.下列能作为比较氧元素和氯元素的非金属性强弱的是( )| A. | H2SO4的酸性比HClO3酸性强 | |
| B. | Fe在纯氧中燃烧生成Fe3O4,Fe在氯气中燃烧生成FeCl3 | |
| C. | 在HClO中,元素化合价氯为+1价,氧为-2价 | |
| D. | O2为无色无味气体,Cl2为黄绿色有刺激性气味的气体 |
分析 元素的非金属性越强,该元素吸引电子能力越强,其单质的氧化性越强,其氢化物的稳定性越强,其单质与氢气反应越容易,其最高价氧化物的水化物酸性越强,据此分析解答.
解答 解:A.H2SO4的酸性比HClO3酸性强,说明硫酸电离程度大于氯酸,与O、Cl非金属性强弱无关,故A错误;
B.一般来说,元素的非金属性越强,对应的单质的氧化性越强,与变价金属反应应生成最高价态,但相同条件下,Cl2与铁反应生成FeCl3,O2与铁反应生成Fe3O4,所以说明氧元素非金属性大于Cl,故B正确;
C.次氯酸中,元素化合价氯为+1价,氧为-2价,说明O元素吸引电子能力大于Cl元素,则非金属性O>Cl,故C正确;
D.非金属性强弱与其单质的颜色无关,故D错误;
故选BC.
点评 本题考查非金属性强弱判断,为高频考点,侧重考查学生分析判断能力及知识综合运用能力,明确非金属性强弱判断方法及与其最高价氧化物的水化物酸性强弱关系、其单质氧化性强弱关系,题目难度不大.

练习册系列答案
相关题目
17.在一定温度下,向2L密闭容器中加入1mol X和2mol Y,发生如下反应:X(g)+2Y(g)?2Z(g),此反应达到平衡的标志是( )
| A. | 容器内气体混合物的密度不随时间变化 | |
| B. | 容器内X、Y、Z浓度之比为1:2:2 | |
| C. | 容器内气体混合物的压强不随时间变化 | |
| D. | 单位时间内消耗0.1mol X,同时生成0.2mol Z |
15.M的名称是乙烯雌酚,它是一种激素类药物,结构简式如图.下列叙述不正确的是( ) 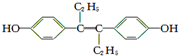

| A. | M的分子式为C18H20O2 | |
| B. | 1 mol M与饱和溴水混合,最多消耗5 mol Br2 | |
| C. | 1 mol M最多能与7 mol H2发生加成反应 | |
| D. | M与NaOH溶液或NaHCO3溶液均能反应 |
2.下列有机物命名正确的是( )
| A. | 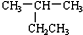 2-乙基丙烷 2-乙基丙烷 | B. | CH3CH═CHCH3 丁烯 | ||
| C. | 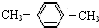 对二甲苯 对二甲苯 | D. | 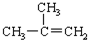 2-甲基-2-丙烯 2-甲基-2-丙烯 |
12.榄香烯是一种新型的抗癌药,它的结构简式如图,有关说法正确的是( )
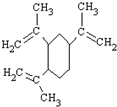

| A. | 榄香烯的分子式为C15H20 | |
| B. | 榄香烯属于芳香烃 | |
| C. | 1 mol 榄香烯最多能和3 mol H2反应 | |
| D. | 榄香烯不能使酸性高锰酸钾溶液和溴的四氯化碳溶液褪色 |
19.戊烷(C5H12)的同分异构体有( )
| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
16.下列过程需要吸收热量的是( )
| A. | 甲烷在空气中燃烧 | B. | 碳酸钙受热分解 | ||
| C. | 镁条溶于盐酸 | D. | 盐酸与氢氧化钠溶液反应 |
17.抗生素药物“芬必得”的主要成分的结构简式如图所示:

下列关于“芬必得”的叙述中正确的是( )

下列关于“芬必得”的叙述中正确的是( )
| A. | 该物质属于不饱和烃 | B. | 该物质的分子式为C13H20O2 | ||
| C. | 该物质属于羧酸类有机物 | D. | 该物质属于芳香烃 |