��Ŀ����
3��������һ����Ҫ�Ļ���ԭ�ϣ����ȼҵ����Ҫ��Ʒ֮һ������һ�ֳ��õ�����������ʵ���ҿ��ö������̺�Ũ���ᷴӦ��ȡ��������Ӧ�Ļ�ѧ����ʽ��MnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O
���ȼҵ���������Ļ�ѧ����ʽΪ2NaCl+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2NaOH+Cl2��+H2��
�����������������䲻���㣬��ҵ�ϳ�������ת��ΪƯ�ۣ���ҵ������Ư�۵���Ҫ��ѧ����ʽ��2Cl2+2Ca��OH��2=CaCl2+Ca��ClO��2+2H2O���ڿ�����Ư�۳��ڴ�Ż���ʶ�ʧЧ��ԭ���ǣ��û�ѧ����ʽ˵����Ca��ClO��2+CO2+H2O=CaCO3+2HClO��2HClO$\frac{\underline{\;����\;}}{\;}$2HCl+O2��
���� �ٶ������̺�Ũ���ᷴӦ�����Ȼ��̡�������ˮ��
���ȼҵ�������������õ�ⱥ��ʳ��ˮ�ķ����õ���
�۹�ҵ���Ʊ�Ư��������ʯ�����������Ӧ�����Ȼ��ơ�������ƺ�ˮ��Ư�۳ɷ�Ϊ�Ȼ��ƺʹ�����ƵĻ�����Ч�ɷ�Ϊ������ƣ�Ư�۳��ڱ�¶�ڿ����л���ʧЧ������Ϊ������ƺͿ����еĶ�����̼��ˮ��Ӧ����̼��Ƴ����ʹ����ᣬ���������ֽ��������������ᣮ
��� �⣺��ʵ����ͨ���ö������̺�Ũ���ᷴӦ��ȡ�����ķ�ӦΪMnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O���ʴ�Ϊ��MnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O��
���ȼҵ�Ʊ����������õ�ⱥ��ʳ��ˮ�ķ����õ�����Ӧ�Ļ�ѧ����ʽΪ��2NaCl+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2NaOH+Cl2��+H2�����ʴ�Ϊ��2NaCl+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2NaOH+Cl2��+H2����
�۹�ҵ���Ʊ�Ư��������ʯ�����������Ӧ�����Ȼ��ơ�������ƺ�ˮ��2Cl2+2Ca��OH��2=CaCl2+Ca��ClO��2+2H2O��Ư�۳ɷ�Ϊ�Ȼ��ƺʹ�����ƵĻ�����Ч�ɷ�Ϊ������ƣ�Ư�۳��ڱ�¶�ڿ����л���ʧЧ������Ϊ������ƺͿ����еĶ�����̼��ˮ��Ӧ����̼��Ƴ����ʹ����ᣬCa��ClO��2+CO2+H2O=CaCO3+2HClO�����������ֽ��������������ᣬ2HClO$\frac{\underline{\;����\;}}{\;}$2HCl+O2����
�ʴ�Ϊ��2Cl2+2Ca��OH��2=CaCl2+Ca��ClO��2+2H2O��Ca��ClO��2+CO2+H2O=CaCO3+2HClO��2HClO$\frac{\underline{\;����\;}}{\;}$2HCl+O2��
���� ���⿼�����������仯�������ʡ������Ʊ���Ư���Ʊ�ԭ����֪ʶ�㣬��Ҫ�ǻ�ѧ����ʽ��д�����ջ����ǽ���ؼ�����Ŀ�ϼ�

| A�� | Al2O3���岻������������ˮ������Al2O3���ǵ���� | |
| B�� | Na2SO4��Һ���磬����Na2SO4�ǵ���� | |
| C�� | ������������磬��������ǵ���� | |
| D�� | 1.5mol/L��NaCl��Һ��1.0mol/L��MgCl2��Һ��Ƚϣ�������������ǿ |
| A�� | �����Ƶij����������ȴ����϶�ͭ����ֹ���� | |
| B�� | ���¸����ܵ�����þ������ֹ������ʴ | |
| C�� | ��������ˢ�����Է��� | |
| D�� | ϴ�»��Ĺ�Ͳ���ò���ֲ��ϡ�����ĥ����ʴ |
| A�� | ʳ������ˮ | B�� | ̼����������ˮ | C�� | ��HClͨ��ˮ�� | D�� | �Ȼ�����ȷֽ� |
| A�� | 1.36��10-5 mol•L-1 | B�� | 8.90��10-6 mol•L-1 | ||
| C�� | 4.45��10-2 mol•L-1 | D�� | 1��10-5 mol•L-1 |
| A�� | ��ɫ������ȫת��Ϊ��ɫ���� | B�� | ���� Ag2S Ҳ�� AgCl | ||
| C�� | �����ɺ�ɫ����ת��Ϊ��ɫ���� | D�� | ֻ�� AgCl ��ɫ���� |
 N��C��SԪ�صĵ��ʼ��������ڹ�ũҵ������������Ҫ��Ӧ��
N��C��SԪ�صĵ��ʼ��������ڹ�ũҵ������������Ҫ��Ӧ����CO��Cl2�ڴ����������ºϳɹ�����COCl2����ij�¶��£���2L���ܱ�������Ͷ��һ������CO��Cl2���ڴ����������·�����Ӧ��CO��g��+Cl2��g��?COCl2��g����Ӧ�����вⶨ�IJ������������
| t/min | n��CO��/mol | n��Cl2��/mol |
| 0 | 1.20 | 0.60 |
| 1 | 0.90 | |
| 2 | 0.80 | |
| 4 | 0.20 |
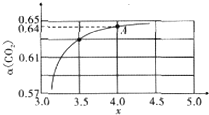
��2��ͼ1��T��ʱ��CO��Cl2�����ʵ���Ũ����ʱ�䣨t���ı仯�������COCl2��ʾ2min�ڵķ�Ӧ����v��COCl2��=0.1mol/��L��min�������¶��µ�ƽ�ⳣ��K=5��
��3����һ�ݻ��ɱ���ܱ������г���10molCO��20molCl2��CO��ƽ��ת�������¶ȣ�T����ѹǿ��P���ı仯��ͼ1��ʾ��
������˵�����жϸ÷�Ӧ�ﵽ��ѧƽ�����BD������ĸ��ţ���
A��Cl2���������ʵ���COCl2����������
B��Cl2�������������
C��Cl2��ת���ʺ�CO��ת�������
D����������ƽ��Ħ���������ٸı�
�ڱȽ�A��B����ѹǿ��С��P��A����P��B�������������������=����
�����ﵽ��ѧƽ��״̬Aʱ�����������Ϊ20L�������Ӧ��ʼʱ�Գ���10molCO��20molCl2������ƽ��״̬Bʱ���������Ϊ4L��
��״���һ����Ҫ�Ļ���ԭ�ϣ������ϣ��״�����ȡ�����������ַ�����
��1������CO��H2��ȡ�״���
��֪CO��CH3OH��H2��ȼ�շֱ���283kj/mol��726.83kj/mol��285.2kj/molд���� CO��H2��ȡ�״����Ȼ�ѧ����ʽCO��g��+2H2��g��=CH3OH��l������H=-126.57kJ/mol��
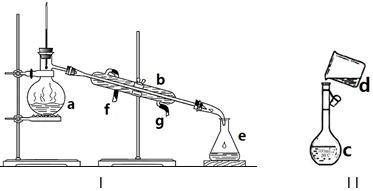
��2���õ绯ѧ����ȡ��ijģ��ֲ�������õĵ绯ѧװ����ͼ2����װ���ܽ�H2O��CO2ת��ΪO2�ͼ״���CH3OH����
�ٸ�װ�ù���ʱH+��b���ƶ����a����b����
��b���ϵĵ缫��ӦʽΪ6H++CO2+6e-=CH3OH+H2O��
 ������Ϊһ�����Է��ϣ������ڸ���������ֲ����ױ��棬ʹ�÷��㣬���������ƻ�����С����Ŀǰʹ�����ϴ��һ�ֻ�ѧ���ʣ�
������Ϊһ�����Է��ϣ������ڸ���������ֲ����ױ��棬ʹ�÷��㣬���������ƻ�����С����Ŀǰʹ�����ϴ��һ�ֻ�ѧ���ʣ�