题目内容
17.下列常见物质的主要成分与化学式相对应的是( )| A. | 光导纤维一Si | B. | 铝土矿一Al2O3 | C. | 磁铁矿一Fe2O3 | D. | 纯碱一NaOH |
分析 A、光导纤维是二氧化硅;
B、铝土矿是氧化铝;
C、磁铁矿是四氧化三铁;
D、纯碱是碳酸钠,据此解答即可.
解答 解:A、光导纤维是二氧化硅,不是硅单质,化学式为:SiO2,故A错误;
B、铝土矿主要含氧化铝,化学式为:Al2O3,故B正确;
C、磁铁矿主要含四氧化三铁,化学式为:Fe3O4,不是Fe2O3,故C错误;
D、纯碱是碳酸钠,化学式为:Na2CO3,故D错误;
故选B.
点评 本题主要考查的是生活中常见化学物质化学式的书写与名称,难度不大,需要认真记忆.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
7.下列有关甲烷、乙烯、苯的说法正确的是( )
| A. | 1mol甲烷和1mol氯气在光照条件下充分反应,生成1mol CH3Cl | |
| B. | 等物质的量的乙烯与碳酸二甲酯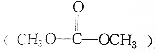 完全燃烧耗氧量相同 完全燃烧耗氧量相同 | |
| C. | 苯和液溴在FeCl3的催化作用下发生加成反应 | |
| D. | 苯在工业上可通过石油分馏得到 |
5.下列有关说法不正确的是( )
| A. | SO42-的空间构型是正四面体形 | |
| B. | CS2分子中各原子均达8电子稳定结构 | |
| C. | 甲醛分子中碳原子的杂化类型为sp2 | |
| D. | CO2与SO2为等电子体 |
12.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 常温常压下,14g由N2和CO组成的混合气体中含有的电子总数为7 NA | |
| B. | 常温下,1 L pH=1的硫酸溶液中含有的H+数目为0.2 NA | |
| C. | 1 L 0.1 mol/L Na2CO3溶液中含有的CO32-数目为0.1 NA | |
| D. | 一定条件下,6.4 g SO2和足量的O2充分反应后,生成SO3的分子数为0.1NA |
2.a mol O2和a mol O3相比较一定相同的是( )
| A. | 体积 | B. | 原子数 | C. | 分子数 | D. | 质量 |
9. 反应A→C分两步进行:①A→B,②B→C.反应过程能量变化曲线如图所示(E1、E2、E3、E4表示活化能).下列说法正确的是( )
反应A→C分两步进行:①A→B,②B→C.反应过程能量变化曲线如图所示(E1、E2、E3、E4表示活化能).下列说法正确的是( )
 反应A→C分两步进行:①A→B,②B→C.反应过程能量变化曲线如图所示(E1、E2、E3、E4表示活化能).下列说法正确的是( )
反应A→C分两步进行:①A→B,②B→C.反应过程能量变化曲线如图所示(E1、E2、E3、E4表示活化能).下列说法正确的是( )| A. | 两步反应的△H均大于0 | B. | 加入催化剂能改变反应的焓变 | ||
| C. | 三种物质中C最稳定 | D. | A→C反应的△H=E4-E1 |
6.下列反应中生成H2的速率最快的是( )
| 金属 | 酸溶液 | 温度 | |
| A | Mg | 0.5mol•L-1 H2SO4 | 20℃ |
| B | Mg | 1mol•L-1 H2SO4 | 30℃ |
| C | Zn | 2mol•L-1 HCl | 20℃ |
| D | Fe | 1mol•L-1 HCl | 20℃ |
| A. | A | B. | B | C. | C | D. | D |
7.化学与生产、生活息息相关,下列叙述错误的是( )
| A. | 寻找合适催化剂提高合成氨工业中原料的转化率 | |
| B. | 对废旧电池进行回收处理,主要是为了环境保护和变废为宝 | |
| C. | 提高油品质量,可以从一定程度上减少雾霾天气 | |
| D. | 含重金属离子的电镀废液不能随意排放 |