题目内容
4.某高分子化合物的部分结构如图:关于该物质的下列说法中,正确的是( )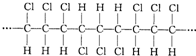
| A. | 合成该聚合物的单体是CHC1=CHC1 | |
| B. | 聚合物的链节(重复的基本结构单元)为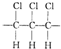 | |
| C. | 聚合物的分子式为C3H3C13 | |
| D. | 该聚合物可表示为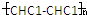 ,其中n为定值 ,其中n为定值 |
分析 从所给结构片断可看出它一直在重复链节 ,因此合成它的单体为CHC1=CHC1,其分子式可表示为
,因此合成它的单体为CHC1=CHC1,其分子式可表示为 CHC1-CHC1
CHC1-CHC1 ,分子式为(C2H2Cl2)n,聚合度n不是定值.
,分子式为(C2H2Cl2)n,聚合度n不是定值.
解答 解:A.该高分子化合物的链节是: ,将两个半键闭合可得其单体:CHCl═CHCl,故A正确;
,将两个半键闭合可得其单体:CHCl═CHCl,故A正确;
B.因为高分子主链上均为C原子,又由于链节是重复的结构单元,且碳碳单键可以旋转,所以该高分子化合物的链节是: ,故B错误;
,故B错误;
C.该聚合物的分子式为:(C2H2Cl2)n,故C错误;
D.该高分子化合物的链节是: ,分子式可表示为
,分子式可表示为 CHC1-CHC1
CHC1-CHC1 ,其中n不是定酯,故D错误;
,其中n不是定酯,故D错误;
故选A.
点评 本题考查对高分子化合物的生成与结构、加聚反应原理,题目难度不大,找准链节是解题的关键,注意高聚物的结构简式、分子式应体现单体,题目难度中等.

练习册系列答案
相关题目
14.用硝酸、硫酸、盐酸、醋酸、钠盐、钾盐、钡盐相互反应,符合离子方程式2H++SO32-=H2O+SO2↑的反应个数有( )
| A. | 4个 | B. | 6个 | C. | 8个 | D. | 12个 |
15.在氨水中存在NH3•H2O?NH4++OH-的平衡,如果要使平衡向左移动,同时使c(OH-)增大,应加入( )
| A. | NH4Cl固体 | B. | H2SO4 | C. | NaOH固体 | D. | 大量水 |
12.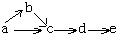 a、b、c、d、e五种物质均含有一种相同的元素,在一定条件下可发生如图所示转化,其中a 是单质;b在通常状况下是气体; c、d都是氧化物;e是该元素的最高价
a、b、c、d、e五种物质均含有一种相同的元素,在一定条件下可发生如图所示转化,其中a 是单质;b在通常状况下是气体; c、d都是氧化物;e是该元素的最高价
氧化物对应水化物,且是一种强电解质,则a可能是( )
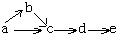 a、b、c、d、e五种物质均含有一种相同的元素,在一定条件下可发生如图所示转化,其中a 是单质;b在通常状况下是气体; c、d都是氧化物;e是该元素的最高价
a、b、c、d、e五种物质均含有一种相同的元素,在一定条件下可发生如图所示转化,其中a 是单质;b在通常状况下是气体; c、d都是氧化物;e是该元素的最高价氧化物对应水化物,且是一种强电解质,则a可能是( )
| A. | N2 | B. | C12 | C. | Si | D. | C |
19.下列物质以任意比混合,只要混合物的质量不变,完全燃烧后产生CO2的质量也不变的是( )
| A. | 乙醛和乙酸乙酯 | B. | 甲酸和乙酸 | ||
| C. | 甲醛和乙醇 | D. | 甲酸甲酯和乙酸乙酯 |
13.在固定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g)?2NH3(g)△H<0,其平衡常数K与温度T的关系如表:
①试判断K1>K2(填写“>”,“=”或“<”)
②下列各项能说明该反应已达到平衡状态的是c(填字母)
a.单位时间内,消耗1molN2的同时生成2mol NH3 b.v(N2)正=3v(H2)逆
c.容器内压强保持不变 d.混合气体的密度保持不变.
| T/K | 298 | 398 | 498 |
| 平衡常数K | 4.1×106 | K1 | K2 |
②下列各项能说明该反应已达到平衡状态的是c(填字母)
a.单位时间内,消耗1molN2的同时生成2mol NH3 b.v(N2)正=3v(H2)逆
c.容器内压强保持不变 d.混合气体的密度保持不变.
14.25℃、1.01×105Pa,下列哪个反应放出的热量表示乙炔的燃烧热(单位:kj•mol-1)( )
| A. | 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(g) | B. | C2H2(g)+$\frac{5}{2}$O2(g)=2CO2(g)+H2O(1) | ||
| C. | C2H2(g)+$\frac{3}{2}$O2(g)=2CO2(g)+H2O(g) | D. | C2H2(g)+$\frac{3}{2}$O2(g)=2CO(g)+H2O(1) |