题目内容
2.一定条件下,将NO2、NO、O2按一定体积比充满一容器,倒置于水槽中,片刻后溶液充满容器,则反应前NO2、NO、O2的体积比为( )①1:1:1 ②4:3:1 ③4:24:19 ④4:24:7 ⑤任意比.
| A. | ① | B. | ②③ | C. | ①④⑤ | D. | ①③ |
分析 若气体能完全溶于水,即NO、NO2、O2三种气体恰好完全反应,全部生成了硝酸,根据反应中电子得失守恒,应该有n(NO)×3+n(NO2)=n(O2)×4,据此对各选项进行判断.
解答 解:若气体能完全溶于水,即NO、NO2、O2三种气体恰好完全反应,全部生成了硝酸,在反应中1molNO失去3mol电子,1molNO2失去1mol电子,1molO2得到4mol电子生成HNO3,根据反应中电子得失守恒,应该有:n(NO2)+n(NO)×3=n(O2)×4成立,相同条件下气体体积与物质的量成正比,则:V(NO2)+V(NO)×3=V(O2)×4,
①1+1×3=4=1×4,故正确;
②4+3×3=13≠1×4=4,故错误;
③4+24×3=76=19×4=76,故正确;
④4+24×3=76≠7×4,故错误;
⑤任意比,故错误;
故选D.
点评 本题主要考查了混合物反应的计算,侧重氧化还原反应中的电子守恒,题目难度中等,掌握反应中电子得失守恒是解题的关键,试题侧重分析能力和计算能力的考查.

练习册系列答案
相关题目
12.下列说法正确的是( )
| A. | 糖类化合物都具有相同的官能团 | |
| B. | 糖类是提供能量最高的营养物质 | |
| C. | 蛋白质的水解产物都含有羧基和氨基 | |
| D. | 酯类在碱性条件下的水解反应称为皂化反应 |
13.下列各组物质的晶体中,所含化学键类型全部相同,熔化时所克服的作用力也完全相同是( )
| A. | CO2和 SiO2 | B. | NaCl 和 HCl | ||
| C. | (NH4)2CO3和 CO(NH2)2(尿素) | D. | NaH 和 KCl |
 R(g)+2L此反应符合下图,
R(g)+2L此反应符合下图,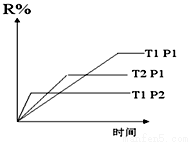
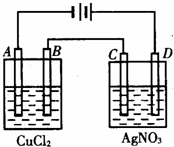 如图为以惰性电极进行电解:
如图为以惰性电极进行电解: