题目内容
 25℃时,在20mL 0.1mol/L NaOH溶液中加入0.2mol/L CH3COOH溶液,所加入溶液的体积(v)和混合液中pH变化关系的曲线如图所示,若B点的横坐标a=10,下列分析的结论正确的是( )
25℃时,在20mL 0.1mol/L NaOH溶液中加入0.2mol/L CH3COOH溶液,所加入溶液的体积(v)和混合液中pH变化关系的曲线如图所示,若B点的横坐标a=10,下列分析的结论正确的是( )| A、在B点有:c(Na+)=c(CH3COO-) |
| B、对曲线上A、B间任何一点,溶液中都有:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
| C、C点时,c(CH3COO-)=c(Na+)>c(H+)=c(OH-) |
| D、D点时,c(CH3COO-)+c(CH3COOH)=c(Na+) |
考点:酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题
分析:A.根据在B点时溶液显示碱性及电荷守恒进行判断钠离子和醋酸根离子浓度大小;
B.根据A、B之间,醋酸少量及醋酸体积稍大的情况进行讨论醋酸根离子与氢氧根离子浓度关系;
C.根据C点pH=7,溶液显示中性进行判断溶液中各离子浓度大小;
D.醋酸浓度是氢氧化钠溶液浓度的2倍,D点时加入醋酸的物质的量为氢氧化钠的物质的量2倍,根据物料守恒进行判断.
B.根据A、B之间,醋酸少量及醋酸体积稍大的情况进行讨论醋酸根离子与氢氧根离子浓度关系;
C.根据C点pH=7,溶液显示中性进行判断溶液中各离子浓度大小;
D.醋酸浓度是氢氧化钠溶液浓度的2倍,D点时加入醋酸的物质的量为氢氧化钠的物质的量2倍,根据物料守恒进行判断.
解答:
解:A.在B点时,溶液pH>7,则c(OH-)>c(H+),根据电荷守恒:c(Na+)+c(H+)=c(CH3COO-)+c(OH-),所以c(Na+)>c(CH3COO-),故A错误;
B.在A、B间任一点,溶液中只存在四种离子有Na+、H+、CH3COO-、OH-,如果加入的醋酸少量,则c(Na+)>c(OH-)>c(CH3COO-)>c(H+),如果加入的醋酸达到一定程度,则会出现c(Na+)>c(CH3COO-)>c(OH-)>c(H+),故B错误;
C.在C点溶液显中性,则c(OH-)=c(H+),根据电荷守恒c(Na+)+c(H+)=c(CH3COO-)+c(OH-),则一定有c(Na+)=c(CH3COO-),溶液中离子浓度大小关系为:c(Na+)=c(CH3COO-)>c(OH-)=c(H+),故C正确;
D.在D点时,醋酸剩余,剩余的醋酸的浓度和生成的醋酸钠浓度相等均为0.05mol/l,根据物料守恒,则:c(CH3COO-)+c(CH3COOH)=0.1mol?L-1,而钠离子浓度为c(Na+)=0.05mol/L,则c(CH3COO-)+c(CH3COOH)=2c(Na+),故D错误;
故选C.
B.在A、B间任一点,溶液中只存在四种离子有Na+、H+、CH3COO-、OH-,如果加入的醋酸少量,则c(Na+)>c(OH-)>c(CH3COO-)>c(H+),如果加入的醋酸达到一定程度,则会出现c(Na+)>c(CH3COO-)>c(OH-)>c(H+),故B错误;
C.在C点溶液显中性,则c(OH-)=c(H+),根据电荷守恒c(Na+)+c(H+)=c(CH3COO-)+c(OH-),则一定有c(Na+)=c(CH3COO-),溶液中离子浓度大小关系为:c(Na+)=c(CH3COO-)>c(OH-)=c(H+),故C正确;
D.在D点时,醋酸剩余,剩余的醋酸的浓度和生成的醋酸钠浓度相等均为0.05mol/l,根据物料守恒,则:c(CH3COO-)+c(CH3COOH)=0.1mol?L-1,而钠离子浓度为c(Na+)=0.05mol/L,则c(CH3COO-)+c(CH3COOH)=2c(Na+),故D错误;
故选C.
点评:本题考查了酸碱混合后的定性判断及溶液中离子浓度大小比较,题目难度中等,注意明确溶液pH与溶液酸碱性的关系,要分清楚每个状态时溶液的组成情况,并注意各种守恒思想的灵活利用.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A、常温常压下,18g H2O含有2NA个O-H键 |
| B、1L 1mol/L Na2CO3溶液中含有NA个CO32- |
| C、1mol Al被完全氧化生成Al2O3,转移6NA个电子 |
| D、常温下,22.4L的N2和O2混合气体,含有2NA个原子 |
能用H++OH-=H2O表示的反应是( )
| A、氢氧化钡溶液与硫酸反应 |
| B、氢氧化铜与稀硝酸反应 |
| C、氢氧化钾与稀盐酸反应 |
| D、氢氧化钠与醋酸溶液反应 |
为把溴水中溴单质萃取出来,应加入( )
| A、苯 | B、苯酚溶液 | C、乙醇 | D、乙醛 |
 天然维生素P(结构如图,其中烃基R为饱和烃基)存在于槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述错误的是( )
天然维生素P(结构如图,其中烃基R为饱和烃基)存在于槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述错误的是( )| A、可以使酸性KMnO4溶液褪色 |
| B、分子中有三个苯环 |
| C、1mol维生素P可以和4mol NaOH反应 |
| D、维生素P与溴水反应时1mol维生素P可以消耗6mol Br2 |
下列说法中不正确的是( )
| A、乙烯与苯都能使溴水褪色,但褪色原理不同 |
| B、1 mol乙烯与Cl2完全加成,然后与Cl2发生取代反应,共消耗氯气5mol |
| C、溴水遇到乙醛溶液出现褪色现象,是因为它们发生了氧化反应 |
D、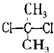 与 与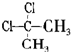 互为同分异构体 互为同分异构体 |
下列叙述中,不正确的是( )
| A、pH=2与pH=1的CH3COOH溶液中,c(H+)之比为1:10 |
| B、1.0mol/L的Na2CO3溶液中:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) |
| C、仅含Na+、H+、OH-、CH3COO-离子的某溶液中可能存在:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| D、0.1mol/L的CH3COOH溶液中,由水电离出的c(H+)为1×10-13mol/L |
 某化学实验室需要0.2mol/L NaOH溶液500mL和0.5mol/L硫酸溶液450mL.根据这两种溶液的配制情况回答下列问题:
某化学实验室需要0.2mol/L NaOH溶液500mL和0.5mol/L硫酸溶液450mL.根据这两种溶液的配制情况回答下列问题: