题目内容
用括号中的试剂和方法除去各组物质中的少量杂质,正确的是( )
| A、苯中的甲苯(酸化高锰酸钾溶液 分液) |
| B、乙醇中的水(无水硫酸铜 干燥) |
| C、乙醇中的乙酸(NaOH溶液 分液) |
| D、苯中的溴:(NaOH溶液 分液) |
考点:物质的分离、提纯和除杂
专题:实验评价题
分析:A.酸性KMnO4可以把甲苯氧化为苯甲酸,苯甲酸与苯互溶;
B.无水硫酸铜吸水能力弱,应用氧化钙;
C.乙醇和乙酸都易溶于水;
D.溴单质能与氢氧化钠反应生成溴化钠和次溴酸钠.
B.无水硫酸铜吸水能力弱,应用氧化钙;
C.乙醇和乙酸都易溶于水;
D.溴单质能与氢氧化钠反应生成溴化钠和次溴酸钠.
解答:
解:A.酸性KMnO4可以把甲苯氧化为苯甲酸,酸性KMnO4与苯不反应,苯甲酸与苯互溶,上层液为苯与苯甲酸,下层为水,不能除去杂质,故A错误;
B.氧化钙可与水反应生成氢氧化钙,乙醇易挥发,可用蒸馏分离,故B错误;
C.乙酸和氢氧化钠反应生成乙酸钠,乙醇和乙酸钠都溶于水,不能分离,故C错误;
D.溴单质能与氢氧化钠反应生成溴化钠和次溴酸钠,然后分液即可,故D正确.
故选D.
B.氧化钙可与水反应生成氢氧化钙,乙醇易挥发,可用蒸馏分离,故B错误;
C.乙酸和氢氧化钠反应生成乙酸钠,乙醇和乙酸钠都溶于水,不能分离,故C错误;
D.溴单质能与氢氧化钠反应生成溴化钠和次溴酸钠,然后分液即可,故D正确.
故选D.
点评:本题考查物质的分离、提纯,为高考常见题型,侧重于学生的分析能力和实验能力的考查,注意把握物质性质的异同,除杂时注意不能引入新的杂质,且不能影响被提纯的物质,难度不大.

练习册系列答案
相关题目
下列实验方法或结论不正确的是( )


| A、可用A装置除去氯气中的氯化氢气体 |
| B、可用B装置量取16.20mL的NaOH溶液 |
| C、可用C实验证明氧化性:Cl2>Br2>S |
| D、可用D装置证明非金属性:S>C>Si |
下列反应属于氧化还原反应的有( )
①CaCO3
CaO+CO2↑
②2KClO3
2KCl+3O2↑
③MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
④2NaCl+H2SO4(浓)
NaSO4+2HCl↑
⑤CuO+H2SO4═CuSO4+H2O
⑥3CuO+2NH3
3Cu+N2+3H2O
⑦Cl2+H2O═HCl+HClO.
①CaCO3
| ||
②2KClO3
| ||
| △ |
③MnO2+4HCl(浓)
| ||
④2NaCl+H2SO4(浓)
| ||
⑤CuO+H2SO4═CuSO4+H2O
⑥3CuO+2NH3
| ||
⑦Cl2+H2O═HCl+HClO.
| A、全部 | B、②③⑥⑦ |
| C、②③⑤⑦ | D、①④⑤⑥ |
下列装置所示的实验中,能达到实验目的是( )
A、 分离碘和酒精 |
B、 除去Cl2中的HCl |
C、 排水法收集NO |
D、 配制硫酸溶液 |
中和相同体积相同pH值的H2SO4、HCl和CH3COOH三种稀溶液中,所用相同浓度的NaOH溶液的体积为V1、V2和V3,则( )
| A、V3>V1=V2 |
| B、V3>V2>V1 |
| C、V1>V2=V3 |
| D、V1>V2>V3 |
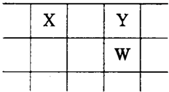 X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素.其中只有Z是金属,W的单质是黄色固体,X、Y、W在周期表中的相对位置关系如图.下列说法不正确的是( )
X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素.其中只有Z是金属,W的单质是黄色固体,X、Y、W在周期表中的相对位置关系如图.下列说法不正确的是( )| A、五种元素中,X最难形成离子化合物 |
| B、五种元素中,Q的最高价含氧酸的酸性强 |
| C、Y的简单阴离子比W的简单阴离子还原性强 |
| D、Z与Q形成的化合物水溶液一定显酸性 |
常温时,下列关于电解质溶液的叙述正确的是( )
| A、稀释pH=10的氨水,溶液中所有离子的浓度均降低 |
| B、pH均为5的盐酸和硫酸氢钠溶液中,水的电离程度相同 |
| C、等物质的量浓度的①NH4HSO4②NH4Cl ③CH3COONH4④(NH4)2SO4c(NH4+)的大小顺序是 ①②③④ |
| D、分别中和pH与体积均相同的硫酸和醋酸,硫酸消耗氢氧化钠的物质的量多 |