题目内容
现实生活中,氨气多用作致冷剂及农用化肥,其实它还是一种清洁能源,在纯氧中可以完全燃烧,只生成水和氮气.最近,科学家用一种含钼的化合物作催化剂,在常温下就能完成氨的合成,从而大大降低了生产成本,使得液氨有望取代液氢成为新一代绿色能源.
(1)N2+3H2═2NH3该反应属于基本反应类型中的 反应.
(2)请你根据下表信息分析用NH3取代H2的优点:
①由于NH3比H2沸点高,所以更易 ,便于储存和运输.
②NH3泄漏时易发现是因为 ,同时它易溶于水,便于处理.
(1)N2+3H2═2NH3该反应属于基本反应类型中的
(2)请你根据下表信息分析用NH3取代H2的优点:
| 性质名称 | 颜色、气味 | 熔点(℃) | 沸点(℃) | 25℃水中溶解度(g/L) | 标况下密度 (g/L) |
| NH3 | 无色、刺激性 | -77.7 | -33 | 456 | 0.6942 |
| H2 | 无色、无味 | -259.2 | -253 | 0.0015 | 0.0899 |
②NH3泄漏时易发现是因为
考点:氨的物理性质
专题:氮族元素
分析:(1)根据化合反应的特点:由多种物质变为一种物质的反应;
(2)①沸点高易液化容易储存;②根据氨气的物理性质考虑.
(2)①沸点高易液化容易储存;②根据氨气的物理性质考虑.
解答:
解:(1)反应物有两种,生成物是一种,所以为化合反应,故答案为:化合;
(2)①沸点高易液化容易储存并且便于运输,故答案为:液化;
②由于氨气具有刺激性气味,所以泄漏后容易觉察到,故答案为:有刺激性气味.
(2)①沸点高易液化容易储存并且便于运输,故答案为:液化;
②由于氨气具有刺激性气味,所以泄漏后容易觉察到,故答案为:有刺激性气味.
点评:本题考查氨气的性质,难度不大,解答本题关键是要知道化合反应的特点,熟悉氨气的性质.

练习册系列答案
相关题目
下列有关化学用语表示正确的是( )
A、比列模型 可以表示二氧化硫分子,也可以表示二氧化碳分子 可以表示二氧化硫分子,也可以表示二氧化碳分子 |
B、电子式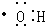 可以表示羟基,也可以表示氢氧根离子 可以表示羟基,也可以表示氢氧根离子 |
C、离子结构示意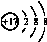 可以表示36Cl-,也可以表示37Cl- 可以表示36Cl-,也可以表示37Cl- |
| D、D结构简式(CH3)2CHOH可以表示1-丙醇,也可以表示2-丙醇 |
用括号中的试剂和方法除去各组物质中的少量杂质,正确的是( )
| A、苯中的甲苯(酸化高锰酸钾溶液 分液) |
| B、乙醇中的水(无水硫酸铜 干燥) |
| C、乙醇中的乙酸(NaOH溶液 分液) |
| D、苯中的溴:(NaOH溶液 分液) |
设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A、常温常压下,15 g甲基(-CH3)所含的电子数为7NA |
| B、水的摩尔质量就是NA个水分子的质量之和 |
| C、含NA个Na+的Na2O2溶于1L水中,Na+的物质的量浓度为1mol/L |
| D、1 mo1Mg与足量O2或N2反应生成MgO或Mg3 N2均失去2NA个电子 |