题目内容
7.中国科学家制得一种蓝色钨的氧化物(WOa),其中钨的质量分数为0.7985.(1)a=2.90(保留2位小数).
(2)WOa中存在五价和六价两种价态的钨.则蓝色钨的氧化物中这两种价态的钨原子数之比为1:4.
将铁锰的钨酸盐[(Fe,Mn)WO4]碱熔,发生如下反应(设空气中N2、O2的体积分数分别为0,.8和0.2):
4FeWO4+4Na2CO3+O2$\stackrel{△}{→}$4Na2WO4+2Fe2O3+4CO2 ①
2MnWO4+2Na2CO3+O2$\stackrel{△}{→}$2Na2WO4+2MnO2+2CO2②
(3)根据反应①,若反应前空气为100L,反应后气体为160L(气体体积在同温同压下测定),则反应后所得气体中CO2的体积分数为50%.
(4)某工厂投料550mol Na2CO3制备Na2WO4,每反应1mol O2时,气体就增加1.5mol,则生成物中Fe2O3与MnO2的物质的量之比为1:3;若反应后气体增加300mol,制得Na2WO4500mol.
(5)由Na2WO4制备W的第一步反应为:Na2WO4+2HCl→H2WO4↓+2NaCl.往1L密度为1,.190g/cm3的37%的浓盐酸加入6.030mol Na2WO4,恰好完全反应.将产生的沉淀过滤后,溶液中溶质只有NaCl,求该溶液中NaCl的质量分数(25℃时NaCl的溶解度为36.0g/100g水):
分析 (1)根据蓝色氧化钨中钨的质量分数为0.7985来计算求出a;
(2)把五价和六价两种价态的氧化物的化学式分别写成WO2.5和WO3,设蓝色氧化钨的组成为xWO2.5•yWO3,利用W和O的个数之比为1:2.90来解答;
(3)若反应前空气为100L,氧气只20L,由4FeWO4+4Na2CO3+O2$\stackrel{△}{→}$4Na2WO4+2Fe2O3+4CO2 生成二氧化碳为80L;
(4)4FeWO4+4 Na2CO3+O2═4 Na2WO4+2Fe2O3+4CO2 气体增加 ①
x 4x 4x 3x
2MnWO4+2Na2CO3+O2═2 Na2WO4+2MnO2+2CO2 气体增加 ②
y 2y 2y y
而每反应1mol O2时,气体就增加1.5mol,由此分析解答;
(5)水的质量为:1000×1.19×0.63=749.7g,生成NaCl为6.030×2×58.5=705.51g;749.7水可溶解NaCl为749.7×0.36=269.90 g,因为是饱和溶液,所以溶液中NaCl的质量分数为=$\frac{36}{136}×100%$.
解答 解:(1)WOa中钨的质量分数为$\frac{183.84}{183.84+16×a}$=0.7985,解得a=2.90;
故答案为:2.90;
(2)把五价和六价两种价态的氧化物的化学式分别写成WO2.5和WO3,设蓝色氧化钨的组成为xWO2.5•yWO3,
因W和O的个数之比为1:2.90,则有$\frac{x+y}{2.5x+3y}=\frac{1}{2.9}$,解得$\frac{x}{y}=\frac{1}{4}$,所以蓝色氧化钨中五价和六价两种价态的钨的原子数之比为:1:4,故答案为:1:4;
(3)若反应前空气为100L,氧气只20L,由4FeWO4+4Na2CO3+O2$\stackrel{△}{→}$4Na2WO4+2Fe2O3+4CO2 生成二氧化碳为80L,所以反应后所得气体中CO2的体积分数为$\frac{80}{160}$×100%=50%,故答案为:50%;
(4)4FeWO4+4 Na2CO3+O2═4 Na2WO4+2Fe2O3+4CO2 气体增加 ①
x 4x 4x 3x
2MnWO4+2Na2CO3+O2═2 Na2WO4+2MnO2+2CO2 气体增加 ②
y 2y 2y y
而每反应1mol O2时,气体就增加1.5mol,所以$\left\{\begin{array}{l}{x+y=1}\\{3x+y=1.5}\end{array}\right.$,解之得:$\left\{\begin{array}{l}{x=0.25}\\{y=0.75}\end{array}\right.$,生成物中Fe2O3与MnO2的物质的量之比为1:3,
则Na2WO4为$\frac{4x+2y}{1.5}×300$=500 mol,故答案为:1:3;500 mol;
(5)水的质量为:1000×1.19×0.63=749.7g,生成NaCl为6.030×2×58.5=705.51g;749.7水可溶解NaCl为749.7×0.36=269.90 g,因为是饱和溶液,所以溶液中NaCl的质量分数为=$\frac{36}{136}×100%$=26.47%,答:该溶液中NaCl的质量分数26.47%.
点评 本题考查根据方程式的计算,题目计算量较大,过程复杂,为易错题目,注意利用关系式与原子守恒进行的解答,难度较大.

| A. | 明矾净水 | B. | 钢铁生锈 | C. | 海水提溴 | D. | 工业固氮 |

| A. | 该分子中存在肽键 | |
| B. | 最多可以有12个碳原子共平面 | |
| C. | 1 mol氯雷他定最多可与8 mol氢气发生加成反应 | |
| D. | 能与NaOH溶液反应,但不能与NaHCO3溶液反应 |
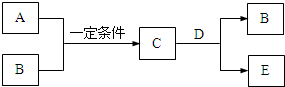 A、B、C、D、E是中学化学中的常见物质,A、B是短周期元素组成的单质.其转化关系如图:
A、B、C、D、E是中学化学中的常见物质,A、B是短周期元素组成的单质.其转化关系如图: 硝酸铜是重要的化工原料,以下三种方法均可得到硝酸铜.
硝酸铜是重要的化工原料,以下三种方法均可得到硝酸铜.