题目内容
15.工业上通过反应“SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑”制取单质硅.下列说法正确的是( )| A. | 自然界中硅元素均以SiO2形式存在 | |
| B. | 高纯度晶体Si可用于制造光导纤维 | |
| C. | 该反应条件下C的还原性比Si强 | |
| D. | 生成4.48LCO时转移电子数为0.4×6.03×1023 |
分析 A.Si是亲氧元素,在自然界中以氧化物或硅酸盐的形式存在;
B.SiO2是制造光导纤维的材料;
C.同一条件下,还原剂的还原性大于还原产物的还原性;
D.温度和压强未知,无法计算CO物质的量.
解答 解:A.Si是亲氧元素,在自然界中以SiO2或硅酸盐的形式存在,故A错误;
B.SiO2是制造光导纤维的材料,Si是制造硅芯片和硅太阳能电池的材料,故B错误;
C.同一条件下,还原剂的还原性大于还原产物的还原性,该反应中C是还原剂、Si是还原产物,所以该反应条件下C的还原性比Si强,故C正确;
D.温度和压强未知,无法计算CO物质的量,导致无法计算转移电子数,故D错误;
故选C.
点评 本题以C和SiO2的反应为载体考查元素化合物性质、基本概念及基本计算,为高频考点,侧重考查学生分析判断及计算能力,知道还原性强弱比较方法,易错选项是D,注意气体摩尔体积适用范围和适用条件,题目难度不大.

练习册系列答案
相关题目
6.下列离子方程式中书写错误的是( )
| A. | AgNO3溶液跟NaCl溶液反应:Ag++Cl-═AgCl↓ | |
| B. | Cl2跟KI溶液反应:Cl2+2I-═I 2+2Cl- | |
| C. | H2SO4跟Ba(OH)2溶液反应H++OH-═H2O | |
| D. | Fe跟FeCl3溶液反应:Fe+2Fe3+═3Fe2+ |
10.溶液X中只可能含有以下离子中的若干种(不考虑盐类的水解及水的电离):K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取100mL溶液X进行如下实验(部分产物省略):
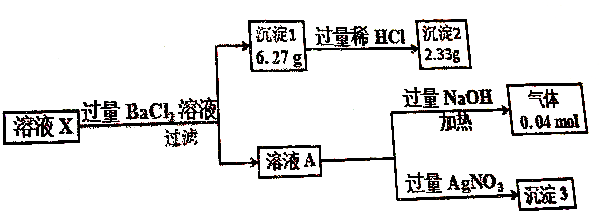
下列说法正确的是( )

下列说法正确的是( )
| A. | 溶液X中存在大量Mg2+ | |
| B. | 溶液X中一定存在K+ | |
| C. | 溶液X中c(CO32-)=0.02mol•L-1 | |
| D. | 溶液X中一定存在NH4+、Cl-、CO32-、SO42- |
20.下列各类物质中,固态时只能形成离子晶体的是( )
| A. | 非金属氧化物 | B. | 非金属单质 | C. | 强酸 | D. | 强碱 |
7.下列离子方程式的书写正确的是( )
| A. | 漂白粉溶液中通入SO2气体 Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO | |
| B. | 碳酸氢钙溶液中加入过量的氢氧化钠溶液 HCO3-+OH-═CO32-+H2O | |
| C. | 明矾溶液中加入过量的Ba(OH)2溶液2Al3++3SO42-+3Ba2++6OH-═3BaSO4↓+2Al(OH)3↓ | |
| D. | 过量的NH4HSO4溶液与Ba(OH)2溶液反应2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O |
4.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 32g氧气所含原子数目为2NA | |
| B. | 在常温常压下,11.2L氯气含有的分子数为0.5NA | |
| C. | 氯化氢的摩尔质量为36.5g | |
| D. | 在标准状况下,22.4L水的物质的量是1mol |
19.下列清洗方法错误的是( )
| A. | 用肥皂洗涤久置石灰水的试剂瓶 | B. | 用酒精清洗残留碘的试管 | ||
| C. | 用洗涤剂清洗餐具上的油污 | D. | 用汽油清洗沾在手上的油漆 |