题目内容
8.设NA为阿伏伽德罗常数的值,下列叙述中正确的是( )| A. | 1molCH3+(甲基正离子)中含有电子数为10NA | |
| B. | 1mol-CH3(甲基)中含有电子数为10NA | |
| C. | 1mol-OH(羟基)与1molOH-所含有电子数相同,均为10NA | |
| D. | 1.8gNH4+中含有的电子数为NA |
分析 A、碳正离子中含有8个电子,1molCH3+(碳正离子)中含有8mol电子;
B、1mol-CH3(甲基)中含有9mol电子;
C、-OH(羟基)与OH-所含电子数分别是9、10;
D、1molNH4+中含有的电子10mol,据m=nM来计算即可.
解答 解:A、碳正离子中含有8个电子,1molCH3+(碳正离子)中含有8mol电子,含有电子数为8NA,故A错误;
B、1mol-CH3(甲基)中含有9mol电子,含有电子数为9NA,故B错误;
C、-OH(羟基)与OH-所含电子数分别是9、10,1mol-OH(羟基)与1molOH-所含有电子数不相同,分别为9NA、10NA,故C错误;
D、1molNH4+中含有的电子10mol,1.8g即0.1molNH4+中含有的电子数为NA,故D正确.
故选D.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,试题题量较大,知识点较多,充分考查了学生对所学知识的掌握情况,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系.

练习册系列答案
相关题目
18.25℃时,两种酸的电离平衡常数如表:
(1)HSO${\;}_{3}^{-}$的电离平衡常数表达式K=$\frac{c(S{{O}_{3}}^{2-})•c({H}^{+})}{c(HS{{O}_{3}}^{-})}$
(2)请根据两种酸的电离平衡常数比较酸陛:H2SO3大于(大于、小于或等于)H2CO3.某同学设计实验比较两者的酸性:将SO2和CO2气体分别通入水中至饱和,立即用酸度计测量两溶液的c(H十).该实验设计不正确,错误在于用于比较pH的两种溶液的物质的量浓度不相等
(3)请用Na2CO3,H2SO4两种溶液,设计方案证明H2SO3和H2CO3的酸性强弱.
操作方法:向盛有亚硫酸溶液的试管中滴加碳酸钠溶液
实验现象:试管中有无色无味的气体产生.
| K1 | K2 | |
| H2SO3 | 1.3×10-2 | 6.3×10-8 |
| H2CO3 | 4.2×10-7 | 5.6×10-11 |
(2)请根据两种酸的电离平衡常数比较酸陛:H2SO3大于(大于、小于或等于)H2CO3.某同学设计实验比较两者的酸性:将SO2和CO2气体分别通入水中至饱和,立即用酸度计测量两溶液的c(H十).该实验设计不正确,错误在于用于比较pH的两种溶液的物质的量浓度不相等
(3)请用Na2CO3,H2SO4两种溶液,设计方案证明H2SO3和H2CO3的酸性强弱.
操作方法:向盛有亚硫酸溶液的试管中滴加碳酸钠溶液
实验现象:试管中有无色无味的气体产生.
3.下列各项中实验目的与实验操作和现象相符的是( )
| 选项 | 实验目的 | 实验操作和现象 |
| A | 检验含Fe2+、Fe3+混合溶液中的Fe2+ | 向溶液中加入足量新制氯水,再加入少量KSCN溶液,溶液变红 |
| B | 检验木炭与浓硫酸反应会生成CO2 | 浓硫酸和木炭混合加热,将生成的气体通入足量澄清石灰水,澄清石灰水变浑浊 |
| C | 验证非金属性:Si<C<Cl | 向Na2CO3固体中加入过量盐酸,将产生的气体直接通入NaSiO3中,产生白色沉淀 |
| D | 验证Ksp[Cu(OH)2]<Ksp[Mg (OH)2] | 向NaOH溶液中滴加足量的MgCl2溶液,产生白色沉淀,在滴加足量的CuCl2溶液,沉淀变蓝色 |
| A. | A | B. | B | C. | C | D. | D |
13.下列各溶液中的离子,因发生氧化还原反应而不能大量共存的是( )
| A. | NH4+、H+、Fe2+、NO3- | B. | K+、NH4+、OH-、SO42- | ||
| C. | Na+、OH-、K+、HCO3- | D. | K+、H+、CH3COO-、NO3- |
20.利用H2、CH3OH、CO等燃料分别构成燃料电池,它们具有的共同特点是( )
| A. | 正、负极均可为惰性电极 | |
| B. | 正极的电极反应式均为O2+2H20+4e-=40H- | |
| C. | 正极通入的气体必须为纯氧气 | |
| D. | 1mol上述燃料完全放电,转移的电子数均为2mol |
5.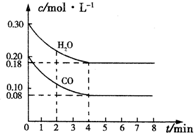 (1)在一容积为10L的容器中,通入一定量的CO和H2O,在850℃时发生反应:CO(g)+H2O(g)═CO2(g)+H2(g)△H<0,
(1)在一容积为10L的容器中,通入一定量的CO和H2O,在850℃时发生反应:CO(g)+H2O(g)═CO2(g)+H2(g)△H<0,
CO和H2O浓度变化如图,则0~4min的平均反应速率v(CO)=0.03mol•L-1•min-1,850℃时,此反应的平衡常数为1,CO的转化率为60%.
(2)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如下表:
①从表中看出,3~4min之间反应处于平衡状态;c1大于0.08(填“大于”、“小于”或“等于”).
②反应在4~5min间,平衡向逆反应方向移动,可能的原因是c,表中5~6min之间数值发生变化,可能的原因是b.
a.降低温度b.增加水蒸气 c.增加氢气浓度d.使用催化剂.
 (1)在一容积为10L的容器中,通入一定量的CO和H2O,在850℃时发生反应:CO(g)+H2O(g)═CO2(g)+H2(g)△H<0,
(1)在一容积为10L的容器中,通入一定量的CO和H2O,在850℃时发生反应:CO(g)+H2O(g)═CO2(g)+H2(g)△H<0,CO和H2O浓度变化如图,则0~4min的平均反应速率v(CO)=0.03mol•L-1•min-1,850℃时,此反应的平衡常数为1,CO的转化率为60%.
(2)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如下表:
| t/min | c(CO)/mol•L-1 | c(H2O)/mol•L-1 | c(CO2)/mol•L-1 | c(H2)/mol•L-1 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
②反应在4~5min间,平衡向逆反应方向移动,可能的原因是c,表中5~6min之间数值发生变化,可能的原因是b.
a.降低温度b.增加水蒸气 c.增加氢气浓度d.使用催化剂.
6.下列物质中存在离子键、共价键和配位键的是( )
| A. | Na2O2 | B. | H3O+ | C. | NH4Cl | D. | NaOH |
 .固体化合物E2D2投入到化合物E2L的水溶液中,只观察到有沉淀产生的,写出该反应的离子方程式为:
.固体化合物E2D2投入到化合物E2L的水溶液中,只观察到有沉淀产生的,写出该反应的离子方程式为: