题目内容
13.下列各溶液中的离子,因发生氧化还原反应而不能大量共存的是( )| A. | NH4+、H+、Fe2+、NO3- | B. | K+、NH4+、OH-、SO42- | ||
| C. | Na+、OH-、K+、HCO3- | D. | K+、H+、CH3COO-、NO3- |
分析 具有还原性的离子与具有氧化性的离子发生氧化还原反应,则不能共存,以此来解答.
解答 解:A.H+、Fe2+、NO3-发生氧化还原反应,不能共存,故A选;
B.NH4+、OH-反应生成一水合氨而不能大量共存,但不是氧化还原反应,故B不选;
C.HCO3-、OH-结合生成水和碳酸根离子,因复分解反应不能共存,故C不选;
D.H+、CH3COO-反应生成醋酸,不是氧化还原反应,故D不选.
故选A.
点评 本题考查离子的共存,为高频考点,把握常见离子的性质及不能共存的原因为解答的关键,涉及水解、复分解、氧化还原反应的考查,题目难度不大.

练习册系列答案
相关题目
4.下列变化不属于化学变化的是( )
| A. | 在稀盐酸中滴入石蕊试液溶液变红 | |
| B. | 少量胆矾粉末加入到浓硫酸中固体变白色 | |
| C. | SO2通入品红中溶液变为无色 | |
| D. | 红糖水中加入活性炭溶液变为无色 |
1.下列按照由大到小排列正确的是( )
| A. | 密度:Cs Rb K Na Li | B. | 溶解度:NaHC03 Na2C03 CaC03 | ||
| C. | 氧化性:Li+Na+K+ Rb+Cs+ | D. | 碱性:LiOH NaOH KOH RbOH CsOH |
8.设NA为阿伏伽德罗常数的值,下列叙述中正确的是( )
| A. | 1molCH3+(甲基正离子)中含有电子数为10NA | |
| B. | 1mol-CH3(甲基)中含有电子数为10NA | |
| C. | 1mol-OH(羟基)与1molOH-所含有电子数相同,均为10NA | |
| D. | 1.8gNH4+中含有的电子数为NA |
5.下列说法正确的是( )
| A. | 得电子越多,其氧化性越强 | |
| B. | 金属活动性顺序表中,排在前面的金属阳离子氧化性强于排在后面的金属阳离子 | |
| C. | SO42-中的硫元素化合价是+6价,处于S元素的最高价态,但SO42-不一定具有强氧化性 | |
| D. | 阳离子只有氧化性,阴离子只有还原性 |
10.下列关于能量变化的说法正确的是( )
| A. | “冰,水为之,而寒于水”说明相同质量的水和冰相比较,冰的能量高 | |
| B. | 化学反应必定同时遵循质量守恒和能量守恒 | |
| C. | 化学反应在物质变化的同时,伴随着能量变化,其表现形式只有吸热和放热两种 | |
| D. | 已知:C(石墨,s)═C(金刚石,s)△H>0,所以金刚石比石墨稳定 |
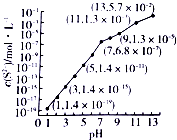 研究硫元素及其化合物的性质具有重要意义.
研究硫元素及其化合物的性质具有重要意义.