题目内容
11.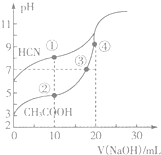 常温下,用0.10mol•L-1 NaOH溶液分别滴定20.00mL浓度均为0.10mol•L-1的CH3COOH溶液和HCN溶液,滴定曲线如图所示.下列说法不正确的是( )
常温下,用0.10mol•L-1 NaOH溶液分别滴定20.00mL浓度均为0.10mol•L-1的CH3COOH溶液和HCN溶液,滴定曲线如图所示.下列说法不正确的是( )| A. | 点①溶液的c(CN-)<点②溶液的c(CH3COO-) | |
| B. | 点②溶液中:c(Na+)+c(H+)=c(CH3COO-)+c(OH-) | |
| C. | 点③溶液中:c(Na+)=c(CH3COO-)+c(CH3COOH) | |
| D. | 点④溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
分析 A.根据点①和点②所示溶液中的电荷守恒分析;
B.根据点②所示溶液中的电荷守恒分析;
C.根据溶液的组成结合物料守恒知识来回答;
D.点④时溶质为醋酸钠,根据点④电荷守恒和溶液的酸碱性判别.
解答 解:A.点①的溶液中存在电荷守恒为c(OH-)+c(CN-)=c(Na+)+c(H+),而且c(OH-)>c(H+),点②所示溶液中的电荷守恒为c(OH-)+c(CH3COO-)=c(Na+)+c(H+),而且c(OH-)<c(H+),二者中钠离子浓度相同,所以点②c(CH3COO-)>点①c(CN-),故A正确;
B.点②所示溶液中存在电荷守恒c(OH-)+c(CH3COO-)=c(Na+)+c(H+),故B正确;
C.点③中滴入的0.10mol•L-1的CH3COOH溶液体积小于20.00mL,溶质为乙酸钠和乙酸,pH=7,c(Na+)<c(CH3COO-)+c(CH3COOH)故C错误;
D.点④溶液中,存在电荷守恒c(OH-)+c(CH3COO-)=c(Na+)+c(H+),c(OH-)>c(H+),则c(CH3COO-)<c(Na+),在④点时加入20mL的氢氧化钠溶液,则此时反应的氢氧化钠的物质的量与醋酸的物质的量相等,溶质为醋酸钠,溶液呈碱性为乙酸钠水解,水解程度较小,所以c(CH3COO-)>c(OH-),即c(Na+)>c(CH3COO-)>c(OH-)>c(H+),故D正确;
故选C.
点评 本题考查酸碱混合溶液中离子浓度的关系,明确混合后溶液中的溶质是解答的关键,注意电荷守恒和物料守恒的应用,题目难度中等.

练习册系列答案
相关题目
1.将Mg、Cu组成的26.4g混合物投入到适量的稀硝酸中,固体完全溶解,将产生的气体和6.72L(标准状况下)氧气混合通入水中,恰好全部被水吸收.向反应后的溶液中加入足量的4mol/L-1的NaOH溶液,使金属离子完全沉淀.则形成沉淀的质量是( )
| A. | 63.8g | B. | 53.6g | C. | 46.8g | D. | 43.2g |
2.下列各组气体中,都能用浓硫酸干燥的是( )
| A. | CO、H2、SO2 | B. | SO2、H2S、O2 | C. | HCl、CO2、H2S | D. | H2、SO2 、NH3 |
19.工业燃烧煤、石油等化石燃料释放出大量氮氧化物(NOx)、CO2、SO2等气体,严重污染空气.对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用.
Ⅰ.脱硝:催化剂存在下,H2还原NO2生成水蒸气和其它无毒物质的化学方程式为4H2+2NO2$\frac{\underline{\;催化剂\;}}{\;}$N2+4H2O.
Ⅱ.脱碳:向2L密闭容器中加入2mol CO2、6mol H2,在恒温恒容的条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0
(1)下列叙述能说明此反应达到平衡状态的是bce.
a.单位时间内生成n mol CH3OH的同时生成n mol H2O
b.CO2和H2的物质的量分数保持不变
c.CO2和H2的浓度保持不变
d.混合气体的密度保持不变
e.生成1mol CO2生成的同时有3mol H-H键断裂
(2)该反应过程中部分数据见下表:
①20min时,反应是否达到平衡状态?是(填“是”或“否”).
简述理由:20min时,n(CH3OH)为1mol,与30min时相同.
②前10min内的平均反应速率v(CH3OH)=0.025mol•L-1•min-1;
平衡时c(H2)=1.5mol/L;平衡时CO2的转化率为50%.
③在其它条件不变下,若20min时向该密闭容器中通入1mol H2,此时该反应速率将增大(填“增大”或“减小”).
Ⅰ.脱硝:催化剂存在下,H2还原NO2生成水蒸气和其它无毒物质的化学方程式为4H2+2NO2$\frac{\underline{\;催化剂\;}}{\;}$N2+4H2O.
Ⅱ.脱碳:向2L密闭容器中加入2mol CO2、6mol H2,在恒温恒容的条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0
(1)下列叙述能说明此反应达到平衡状态的是bce.
a.单位时间内生成n mol CH3OH的同时生成n mol H2O
b.CO2和H2的物质的量分数保持不变
c.CO2和H2的浓度保持不变
d.混合气体的密度保持不变
e.生成1mol CO2生成的同时有3mol H-H键断裂
(2)该反应过程中部分数据见下表:
| 反应时间 | CO2 (mol) | H2 (mol) | CH3OH (mol) | H2O (mol) |
| 0min | 2 | 6 | 0 | 0 |
| 10min | 4.5 | |||
| 20min | 1 | |||
| 30min | 1 |
简述理由:20min时,n(CH3OH)为1mol,与30min时相同.
②前10min内的平均反应速率v(CH3OH)=0.025mol•L-1•min-1;
平衡时c(H2)=1.5mol/L;平衡时CO2的转化率为50%.
③在其它条件不变下,若20min时向该密闭容器中通入1mol H2,此时该反应速率将增大(填“增大”或“减小”).
16.化学与生活密切相关,下列说法不正确的是( )
| A. | 葡萄糖中的花青素在碱性环境下显蓝色,故可用苏打粉辨别真假葡萄酒 | |
| B. | 氨氮废水(含NH4+及NH3)可用化学氧化法或电化学氧化法处理 | |
| C. | 金属的防护中,牺牲阳极的阴极保护法利用的是原电池原理 | |
| D. | 84消毒液在日常生活中广泛应用,其有效成分是Ca(ClO)2 |
3.燃料电池是燃料(如甲烷等)跟O2(或空气)起反应将化学能转变为电能的装置,电解质溶液是强碱(如KOH )溶液,下列关于甲烷燃料电池的说法中不正确的是( )
| A. | 负极的电极反应式为:CH4+10OH--8e-═CO32-+7H2O | |
| B. | 通入氧气的一极发生氧化反应,通入甲烷的一极发生还原反应 | |
| C. | 随着反应的进行,电解质溶液的pH增大 | |
| D. | 甲烷燃料电池的能量利用率比甲烷燃烧的大 |
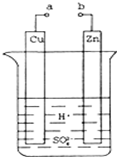 原电池是化学对人类的一项重大贡献.某兴趣小组为研究原电池原理,设计如图装置:
原电池是化学对人类的一项重大贡献.某兴趣小组为研究原电池原理,设计如图装置: