题目内容
有X、Y、Z、W四种元素,已知:
①它们都是短周期元素,X和Z在同一主族;
②Y和Z可以组成Z2Y、Z2Y2等化合物;
③WY3与水化合生成一种强酸,此强酸与Z2W反应生成一种气体X2W,根据以上推断回答下列问题:
(1)X、Y、Z、W四种元素符号依次为 .
(2)画出W2-的结构示意图 .
(3)用电子式表示气体X2W的形成过程 .用电子式表示Z2W的形成过程 .
(4)W3Y与水化合生成的强酸与Z2W反应的离子方程式为 .
(5)如图为A、Y单质形成的燃料电池结构示意图.

①A物质的化学式是 .
②供电时的总反应是 .
①它们都是短周期元素,X和Z在同一主族;
②Y和Z可以组成Z2Y、Z2Y2等化合物;
③WY3与水化合生成一种强酸,此强酸与Z2W反应生成一种气体X2W,根据以上推断回答下列问题:
(1)X、Y、Z、W四种元素符号依次为
(2)画出W2-的结构示意图
(3)用电子式表示气体X2W的形成过程
(4)W3Y与水化合生成的强酸与Z2W反应的离子方程式为
(5)如图为A、Y单质形成的燃料电池结构示意图.

①A物质的化学式是
②供电时的总反应是
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:X、Y、Z、W都是短周期元素,Y和Z可以组成Z2Y、Z2Y2等化合物,则Y为氧元素,Z为氢元素或钠元素,WY3与水化合生成一种强酸,则W为硫元素,此强酸与Z2W反应生成一种气体X2W,X和Z在同一主族,则Z为钠元素,X为氢元素,据此答题;
解答:
解:X、Y、Z、W都是短周期元素,Y和Z可以组成Z2Y、Z2Y2等化合物,则Y为氧元素,Z为氢元素或钠元素,WY3与水化合生成一种强酸,则W为硫元素,此强酸与Z2W反应生成一种气体X2W,X和Z在同一主族,则Z为钠元素,X为氢元素,
(1)根据上面的分析可知,X、Y、Z、W四种元素符号依次为H、O、Na、S,故答案为:H、O、Na、S;
(2)S2-的结构示意图为 ,故答案为:
,故答案为: ;
;
(3)H2S为共价化合物,用电子式表示气体H2S的形成过程为 ,Na2S为离子化合物,用电子式表示Na2S的形成过程为
,Na2S为离子化合物,用电子式表示Na2S的形成过程为 ,故答案为:
,故答案为: ;
; ;
;
(4)硫酸与硫化钠反应的离子方程式为S2-+2H+=H2S↑,故答案为:S2-+2H+=H2S↑;
(5)①根据图可知,电解质溶液中由负极流向正极的为氢离子,所以A物质应为氢气,故答案为:H2;
②供电时的总反应为2H2+O2=2H2O,故答案为:2H2+O2=2H2O;
(1)根据上面的分析可知,X、Y、Z、W四种元素符号依次为H、O、Na、S,故答案为:H、O、Na、S;
(2)S2-的结构示意图为
 ,故答案为:
,故答案为: ;
;(3)H2S为共价化合物,用电子式表示气体H2S的形成过程为
 ,Na2S为离子化合物,用电子式表示Na2S的形成过程为
,Na2S为离子化合物,用电子式表示Na2S的形成过程为 ,故答案为:
,故答案为: ;
; ;
;(4)硫酸与硫化钠反应的离子方程式为S2-+2H+=H2S↑,故答案为:S2-+2H+=H2S↑;
(5)①根据图可知,电解质溶液中由负极流向正极的为氢离子,所以A物质应为氢气,故答案为:H2;
②供电时的总反应为2H2+O2=2H2O,故答案为:2H2+O2=2H2O;
点评:本题主要考查了根据元素组成的化合物的性质推断元素种类,并在此基础上进一步考查了物质结构、离子反应、电化学的有关知识,中等难度.

练习册系列答案
相关题目
实验室有一瓶混有氯化钠的氢氧化钠固体试剂,经测定NaOH的质量分数为82.0%,为了验证其纯度,用浓度为0.2mol?L-1的盐酸进行滴定,结果偏高,试分析可能由下列哪些实验操作引起的( )
| A、转移待测液至容量瓶时,未洗涤烧杯 |
| B、滴定到终点时,滴定管尖嘴悬有液滴 |
| C、滴定时,反应容器摇动太激烈,有少量液体溅出 |
| D、读酸式滴定管开始时仰视,读终点时俯视 |
W、X、Y、Z是短周期元素,其部分性质如表,下列说法正确的是( )
| W | 单质是淡黄色固体 | ||
| X | 在地壳中的含量居第二位 | ||
| Y | 原子最外层电子数是电子总数的
| ||
| Z | 第三周期原子半径最小的金属 |
| A、气态氢化物的热稳定性:X<W |
| B、最高价氧化物对应水化物的酸性:Y>X |
| C、离子半径:Z>W |
| D、Y的氧化物中含有非极性共价键 |
下列包装标识贴错了的是( )
| 选项 | A | B | C | D |
| 物质 | 浓硫酸 | 酒精 | 小苏打 | 氯酸钾 |
| 标识 |  |  |  |  |
| A、A | B、B | C、C | D、D |
目前,科学家正在研究开发一种高能电池--钠硫电池,它以熔融钠、硫为两极,以导电的β-A2lO3陶瓷作固体电解质,反应式如下:Na2SX
2Na+xS以下说法正确的是( )
| ||
| 放电 |
| A、放电时,Na作正极,S极发生还原反应 |
| B、放电时,Na发生还原反应 |
| C、充电时,钠极与外电源的正极相连 |
| D、充电时,阳极发生的反应为:SX2--2e=xS |
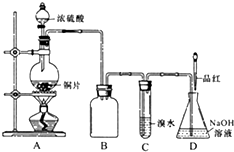 某化学兴趣小组设计实验,用浓硫酸与铜反应制得SO2并进行相关实验探究.
某化学兴趣小组设计实验,用浓硫酸与铜反应制得SO2并进行相关实验探究.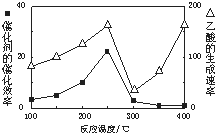 CH4和CO2反应可以制造价值更高的化学产品.
CH4和CO2反应可以制造价值更高的化学产品.