题目内容
6.下列有关实验的叙述正确的是( )| A. | 将一定量的氯气通入30 mL浓度为10.0mol/L的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3共存体系,n(NaCl):n(NaClO):n(NaClO3)可能为11:2:1 | |
| B. | 实验室可以配制一种仅含Al3+、K+、SO42-、NO3-这4种离子(不考虑来源于水电离的离子)的溶液,且4种离子的浓度均为1mol/L | |
| C. | HCl、FeCl3、Fe3O4、NaOH都可通过置换反应一步得到也可通过化合反应一步得到 | |
| D. | 实验室制氢气,为了加快反应速率,可向稀H2SO4中滴加少量Cu(NO3)2溶液 |
分析 A.n(NaCl):n(NaClO):n(NaClO3)可能为11:2:1,则得到电子数为11,失去电子数为2×1+1×5=7;
B.4种离子的浓度均为1mol/L,阳离子电荷总数大于阴离子电荷总数;
C.HCl可以2HBr+Cl2=2HCl+Br2置换反应得到,H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl为化合反应;2FeBr3+3Cl2=3Br2+2FeCl3为置换反应,Cl2+2FeCl2=2FeCl3为化合反应;3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2为置换反应,3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4为化合反应;NaOH可以2Na+2H2O=2NaOH+H2↑置换反应得到,H2O+Na2O=2NaOH为化合反应;
D.向稀H2SO4中滴加少量Cu(NO3)2溶液,酸性溶液中硝酸根离子具有强氧化性,与金属反应不生成氢气.
解答 解:A.n(NaCl):n(NaClO):n(NaClO3)可能为11:2:1,则得到电子数为11,失去电子数为2×1+1×5=7,则转移电子不守恒,与氧化还原反应的实质不一致,故A错误;
B.4种离子的浓度均为1mol/L,阳离子电荷总数大于阴离子电荷总数,与溶液为电中性不一致,故B错误;
C.2HBr+Cl2=2HCl+Br2、2FeBr3+3Cl2=3Br2+2FeCl3、3Fe+4H2O(g)$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2、2Na+2H2O=2NaOH+H2↑均为置换反应一步得到,H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl、Cl2+2FeCl2=2FeCl3、3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4、H2O+Na2O=2NaOH均为化合反应一步得到,故C正确;
D.向稀H2SO4中滴加少量Cu(NO3)2溶液,酸性溶液中硝酸根离子具有强氧化性,与金属反应不生成氢气,则不能加硝酸铜,可加硫酸铜构成原电池加快反应速率,故D错误;
故选C.
点评 本题考查较综合,涉及氧化还原反应、电荷守恒、元素化合物性质及转化、反应速率等,综合性较强,注重高频考点的考查,题目难度中等,选项C为解答的难点.

| A. | 同主族元素含氧酸的酸性随核电荷数的增加而减弱 | |
| B. | 核外电子排布相同的微粒化学性质也相同 | |
| C. | 同主族元素从上到下,单质的熔点逐渐降低 | |
| D. | 同族上下相邻两种元素的原子序数之差可能为32 |
| A. | H2 | B. | Cl2 | C. | N2 | D. | O2 |
| A. | 马口铁(镀锡铁)镀层受损后,铁制品比受损前更容易生锈 | |
| B. | 2CaCO3(s)+2SO2(g)+O2(g)═2CaSO4(s)+2CO2(g)在高温下能自发进行,则该反应的△H>0 | |
| C. | 恒温恒容密闭容器中进行的反应N2(g)+3H2(g)?2NH3(g);△H=a kJ•mol-1,平衡时向容器中再充入N2和H2,反应速率加快,a值不变 | |
| D. | 氢硫酸(弱酸)中加入少量CuSO4溶液(H2S+CuSO4═CuS↓+H2SO4),H2S的电离程度和溶液的pH均增大 |
| 实 验 事 实 | 结 论 | |
| A | Cl2的水溶液可以导电 | Cl2是电解质 |
| B | 将燃烧的镁条放入CO2中能继续燃烧 | 还原性:Mg>C |
| C | 将Na2CO3溶液与苯酚浊液混合溶液变澄清 | 酸性:苯酚>HCO3- |
| D | 常温下白磷可自燃而氮气须在放电时才与氧气反应 | 非金属性:P>N |
| A. | A | B. | B | C. | C | D. | D |
| A. | 乙烯和苯都能使溴水褪色,褪色的原因相同 | |
| B. | 甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应 | |
| C. | 葡萄糖和果糖的分子式均为C6H12O6,二者互为同系物 | |
| D. | 乙醇、乙酸、乙酸乙酯都能发生取代反应,乙酸乙酯中的少量乙酸可用饱和Na2CO3溶液除去 |
| A. | 质量数为293的117号元素原子中质子数比中子数多176 | |
| B. | 117号元素是非金属元素 | |
| C. | ${\;}_{20}^{48}$Ca、${\;}_{20}^{40}$Ca 互称同位素 | |
| D. | 预测${\;}_{117}^{293}$X、${\;}_{117}^{294}$X 性质相同(用X表示117号元素的符号) |
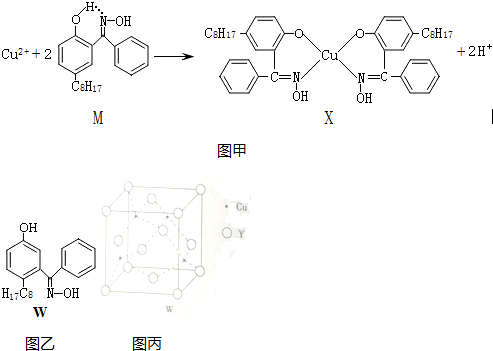
(1)X难溶于水、易溶于有机溶剂,其晶体类型为分子晶体.
(2)M所含元素的电负性由大到小顺序为O>N>C>H,分子中碳原子的杂化方式有sp2、sp3.
(3)上述反应中断裂和生成的化学键有be(填序号).
a.离子键 b.配位键 c.金属键 d.范德华力 e.共价键
(4)M与W(分子结构如图乙)相比,M的水溶性小,更利于Cu2+的萃取.M水溶性小的主要原因是M能形成分子内氢键,使溶解度减小.
(5)基态Cu2+的外围电子排布式为3d9,Cu2+等过渡元素水合离子是否有颜色与原子结构有关,且存在一定的规律.判断Sc3+、Zn2+的水合离子为无色的依据是3d轨道上没有未成对电子(3d轨道上电子为全空或全满).
| 离子 | Sc3+ | Ti3+ | Fe2+ | Cu2+ | Zn2+ |
| 颜色 | 无色 | 紫红色 | 浅绿色 | 蓝色 | 无色 |
①晶体的化学式是CuCl.
②已知该晶体的密度为ρg•cm-3,阿伏伽德罗常数的值为NA,则该晶体中铜原子与Y原子之间的最短距离为=$\frac{\sqrt{3}}{4}\root{3}{\frac{4×99.5}{ρ{N}_{A}}}$×1010pm(只写计算式).