题目内容
8.下列物质中,既能导电又属于电解质的是( )| A. | 蔗糖 | B. | 熔融的氯化钠 | C. | 氯化氢气体 | D. | 锌片 |
分析 电解质是水溶液中或熔融状态下都导电的化合物;
非电解质是在水溶液和熔融状态下都不导电的化合物;
物质导电的条件:存在自由电子或者自由移动的离子,据此解答.
解答 解:A.蔗糖在水溶液和熔融状态下都不导电,属于非电解质,故A错误;
B.熔融的氯化钠含有自由移动的离子,能够导电,是水溶液中或熔融状态下都导电的化合物,属于电解质,故B正确;
C.氯化氢是电解质,但是不含有自由电子或者自由移动的离子,不导电,故C错误;
D.锌含有自由电子能够导电,是单质,既不是电解质也不是非电解质,故D错误;
故选:B.
点评 本题考查了电解质的判断,熟悉电解质的概念是解题关键,注意电解质一定是化合物,单质、混合物既不是电解质,也不是非电解质.

练习册系列答案
相关题目
18.下列物质的稀溶液中,除水分子外,存在其它分子的是( )
| A. | NaCl | B. | NaOH | C. | HNO3 | D. | HClO |
19.下列溶液中的Cl-浓度与50mL0.5mol•L-1 MgCl2溶液中的Cl-浓度相等的是( )
| A. | 50 mL 1 mol•L-1 NaCl溶液 | B. | 100 mL 0.5mol•L-1CaCl2溶液 | ||
| C. | 150 mL 1 mol•L-1 CuCl2溶液 | D. | 75 mL 1 mol•L-1AlCl3溶液 |
13.二氧化碳和钠在一定条件下可制得金刚石,其化学方程式为3CO2+4Na=2X+C(金刚石).设NA为阿伏加德罗常数的值,下列有关此反应的叙述不正确的是( )
| A. | 金刚石是自然界最坚硬的单质 | |
| B. | 1 mol CO2中含有的共用电子对数目为2NA | |
| C. | 46g Na完全反应需要标准状况下CO2的体积为33.6L | |
| D. | 当有0.4mo1 Na参与反应时,被还原的CO2的分子数目为0.1 NA |
20.由-CH3、-OH、 、-COOH四种基团两两组合而成的化合物中,其水溶液能使石蕊变红的有( )
、-COOH四种基团两两组合而成的化合物中,其水溶液能使石蕊变红的有( )
 、-COOH四种基团两两组合而成的化合物中,其水溶液能使石蕊变红的有( )
、-COOH四种基团两两组合而成的化合物中,其水溶液能使石蕊变红的有( )| A. | 5种 | B. | 4种 | C. | 3种 | D. | 2种 |
18.某无色透明溶液中,能够大量共存的离子组是( )
| A. | Na+、K+、MnO4-、NO3- | B. | Na+、Ba2+、OH-、CO32- | ||
| C. | Fe2+、H+、SO42-、NO3- | D. | Mg2+、Na+、NO3-、SO42- |
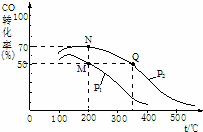 减少污染、保护环境是全世界最热门的课题.请回答下列问题:
减少污染、保护环境是全世界最热门的课题.请回答下列问题: