题目内容
17.用Cr3+掺杂的氮化铝是理想的LED用荧光粉基质材料,氮化铝(其晶胞如图1所示)可由氯化铝与氨经气相反应制得.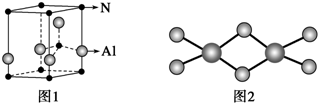
(1)Cr3+基态的核外电子排布式可表示为1s22s22p63s23p63d3.
(2)氮化铝的化学式为AlN.
(3)氯化铝是易升华,其双聚物Al2Cl6结构如图2所示.在Al2Cl6中存在的化学键有bc(填字母).
a.离子键 b.共价键 c.配位键 d.金属键
(4)一定条件下用Al2O3和CCl4反应制备AlCl3的反应为Al2O3+3CCl4═2AlCl3+3COCl2.其中,COCl2分子的空间构型为平面三角形.
分析 (1)铬24号元素,铬元素失去3个电子变成Cr3+,所以Cr3+核外有21个电子,根据构造原理写出其核外电子排布式;
(2)利用均摊法求出晶胞中两种原子的个数,再确定分子式;
(3)根据双聚物Al2Cl6结构确定化学键的类型;
(4)COCl2分子的结构式为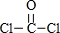 ,双键中含有1个δ键、1个π键,确定碳原子的杂化方式与分子构型.
,双键中含有1个δ键、1个π键,确定碳原子的杂化方式与分子构型.
解答 解:(1)铬24号元素,铬元素失去3个电子变成Cr3+,所以Cr3+核外有21个电子,根据构造原理知,该离子核外电子排布式为:1s22s22p63s23p63d3,
故答案为:1s22s22p63s23p63d3;
(2)氮化铝晶胞中N原子的个数=8×$\frac{1}{8}$+1=2,Al原子的个数=4×$\frac{1}{4}$+1=2,所以氮化铝的化学式为AlN;
故答案为:AlN;
(3)双聚物Al2Cl6形式存在,氯化铝中铝原子最外层电子只有3个电子,每个铝原子和四个氯原子形成共价键,且其中一个共用电子对是氯原子提供,所以含有配位键,则在Al2Cl6中存在的化学键有共价键、配位键,
故答案为:bc;
(4)COCl2分子的结构式为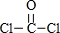 ,C=O中含有1个δ键、1个π键,碳原子的杂化方式为SP2杂化,分子的空间构型为平面三角形;
,C=O中含有1个δ键、1个π键,碳原子的杂化方式为SP2杂化,分子的空间构型为平面三角形;
故答案为:平面三角形.
点评 本题考查物质结构,涉及化学式的确定、杂化方式的确定、核外电子排布式的书写等知识,利用均摊法、价层电子对互斥理论、构造原理来分析解答即可,题目难度中等.

练习册系列答案
相关题目
8.下列物质中,既能导电又属于电解质的是( )
| A. | 蔗糖 | B. | 熔融的氯化钠 | C. | 氯化氢气体 | D. | 锌片 |
5.2008年北京奥运会的“祥云”火炬所用的燃料的主要成分是丙烷,下列有关丙烷的叙述中不正确的是( )
| A. | 分子中碳原子不在一条直线上 | B. | 光照下能够发生取代反应 | ||
| C. | 正丁烷的沸点比丙烷低 | D. | 丙烷不存在同分异构体 |
2.对于铝热反应:Fe2O3+2Al$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3,下列说法中正确的是( )
| A. | Fe元素的化合价升高 | |
| B. | 若27 g Al参加反应则有3 mol电子转移 | |
| C. | Fe2O3发生氧化反应 | |
| D. | Al被还原 |
6.下列实验操作中,正确的是( )
| A. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 | |
| B. | 用蒸发的方法使NaCl从溶液中析出时,应将蒸发皿中NaCl溶液全部加热蒸干 | |
| C. | 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| D. | 用试管取出试剂瓶中的Na2CO3溶液,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中 |
7.下列叙述错误的是( )
(1)石油裂解、煤的气化、溶液导电都属于化学变化
(2)H2S水溶液是弱酸,HCl水溶液是强酸,可以验证硫元素的非金属性比氯元素弱
(3)H2O、H2S、H2Se的相对分子质量增大,所以熔沸点依次升高
(4)液态氟化氢中存在氢键,所以其分子比氯化氢更稳定
(5)都是由非金属元素形成的化合物只能是共价化合物.
(1)石油裂解、煤的气化、溶液导电都属于化学变化
(2)H2S水溶液是弱酸,HCl水溶液是强酸,可以验证硫元素的非金属性比氯元素弱
(3)H2O、H2S、H2Se的相对分子质量增大,所以熔沸点依次升高
(4)液态氟化氢中存在氢键,所以其分子比氯化氢更稳定
(5)都是由非金属元素形成的化合物只能是共价化合物.
| A. | 全部 | B. | (2)(3)(4) | C. | (1)(2)(3)(5) | D. | (2)(3)(4)(5) |
 目前城市空气质量恶化原因之一是机动车尾气和燃煤产生的烟气.NO和CO均为汽车尾气的成分,这两种气体在催化转换器中发生如下反应:
目前城市空气质量恶化原因之一是机动车尾气和燃煤产生的烟气.NO和CO均为汽车尾气的成分,这两种气体在催化转换器中发生如下反应: