题目内容
如图表示汽车尾气净化处理过程.有关叙述正确的是( )
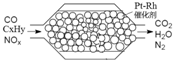

| A、产生22.4L氮气(标准状况)时,转移4x mol e- |
| B、上述过程中,NOx只被CO还原 |
| C、安装该净化器的汽车使用含铅汽油不会造成污染 |
| D、Pt-Rh催化剂可提高尾气的平衡转化率 |
考点:氮的氧化物的性质及其对环境的影响
专题:氮族元素
分析:A.根据生成1个氮气分子会转移4x个电子来分析;
B.根据元素化合价变化判断物质发生的反应;
C.根据安装这种净化器,不能减少铅的排放来回答;
D.根据催化剂只能改变反应速率,不能改变平衡移动.
B.根据元素化合价变化判断物质发生的反应;
C.根据安装这种净化器,不能减少铅的排放来回答;
D.根据催化剂只能改变反应速率,不能改变平衡移动.
解答:
解:A.产生22.4L氮气即1mol(标准状况)时,转移4xmol e-,故A正确;
B.该反应过程中,CO和CxHy均失电子而作还原剂,NOX被CO和CxHy还原,故B错误;
C.安装这种净化器,不能减少铅的排放,所以仍然造成铅污染,故C错误;
D.催化剂只能改变反应速率,不能改变平衡移动,所以不能提高尾气平衡转化率,故D错误;
故选:A.
B.该反应过程中,CO和CxHy均失电子而作还原剂,NOX被CO和CxHy还原,故B错误;
C.安装这种净化器,不能减少铅的排放,所以仍然造成铅污染,故C错误;
D.催化剂只能改变反应速率,不能改变平衡移动,所以不能提高尾气平衡转化率,故D错误;
故选:A.
点评:本题考查氧化还原反应、外界条件对速率和平衡的影响,明确元素化合价是解本题关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列实验操作中叙述不正确的是( )
| A、进行蒸馏操作时先加热再通冷凝水 |
| B、分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
| C、容量瓶用蒸馏水洗涤后不烘干就使用 |
| D、为了便于操作,浓溶液稀释或固体溶解可直接在容量瓶中进行 |
 向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以
向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以 | 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5L | 0.5L | 1.0L |
| 温度/℃ | T1 | T2 | T2 |
| 反应物 起始量 | 1.5mol A 0.5mol B | 1.5mol A 0.5mol B | 6.0mol A 2.0mol B |
| A、10min内甲容器中反应的平均速率:v(A)=0.05mol?(L?min)-1 |
| B、由图可知T1>T2,且该反应为吸热反应 |
| C、x=1,若平衡时保持温度不变,改变容器体积平衡不移动 |
| D、T2℃,丙容器比乙容器反应快的原因可能是使用了催化剂 |
下列说法正确的是( )
| A、在化学反应中,分子可以再分,离子、原子不可以再分 |
| B、同一种元素可能含有多种不同的原子,同一种原子也可能形成不同的离子 |
| C、分子是保持物质化学性质的唯一微粒 |
| D、质子数、中子数和电子数都相同的微粒一定是同一种粒子 |
下列叙述不正确的是( )
| A、可用溴水鉴别直馏汽油与裂化汽油 |
| B、铜丝灼烧法可定性确定有机物中是否存在卤素 |
| C、德国化学家维勒提出了有机化学的概念 |
| D、CH3CH=CHCH(CH3)CH=CHCH3中不存在对映异构体,但存在顺反异构 |
X、Y、Z、T四种原子序数递增的短周期元素,其部分性质或结构如下:
下列说法正确的是( )
| 元素编号 | 元素性质或原子结构 |
| X | 形成的简单阳离子核外无电子 |
| Y | 元素的气态氢化物和它的最高价氧化物对应的水化物能发生化合反应 |
| Z | 元素在周期表的族序数等于周期序数的3倍 |
| T | 同周期元素中形成的简单离子半径最小 |
| A、原子半径大小顺序:T>Z>Y>X |
| B、X、Y、Z三种元素可形成既含共价键又含离子键的化合物 |
| C、T的单质与Y的最高价氧化物对应水化物的溶液不反应 |
| D、由X、Y和Z三种元素构成的强电解质,对水电离均起抑制作用 |
 则乙醇发生酯化反应时,断裂的键是
则乙醇发生酯化反应时,断裂的键是 ②CH2=CH2③CH≡CH ④
②CH2=CH2③CH≡CH ④ -CH2OH⑤
-CH2OH⑤ -CH3⑥CH3COO-
-CH3⑥CH3COO- ⑦CH3CH2CH2CH2Br中属于芳香烃的是
⑦CH3CH2CH2CH2Br中属于芳香烃的是