题目内容
等物质的量的下列有机物完全燃烧,消耗O2最多的是( )
| A、CH4 |
| B、C2H4 |
| C、CH3CH2OH |
| D、C3H8 |
考点:化学方程式的有关计算
专题:烃及其衍生物的燃烧规律
分析:CH3CH2OH可以改写为C2H4?H2O,看作乙烯与水的混合物,烃的化学式为CxHy,1mol烃消耗的氧气的物质的量为(x+
)mol,据此判断.
| y |
| 4 |
解答:
解:A.1molCH4耗氧量为:(1+
)mol=2mol;
B.1molC2H4耗氧量为:(2+
)mol=3mol;
C.CH3CH2OH可以改写为C2H4?H2O,1molC2H4耗氧量为:(2+
)mol=3mol;
D.1molC3H8耗氧量为:(3+
)mol=5mol,
故等物质的量耗氧量最多的是C3H8,
故选:D.
| 4 |
| 4 |
B.1molC2H4耗氧量为:(2+
| 4 |
| 4 |
C.CH3CH2OH可以改写为C2H4?H2O,1molC2H4耗氧量为:(2+
| 4 |
| 4 |
D.1molC3H8耗氧量为:(3+
| 8 |
| 4 |
故等物质的量耗氧量最多的是C3H8,
故选:D.
点评:本题考查烃完全燃烧耗氧量问题,难度不大,利用烃的燃烧通式明确相同物质的量的烃CxHy完全燃烧耗氧量取决(x+
),注意将烃的含氧衍生物改写烃与水的形式简化计算.
| y |
| 4 |

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
在强碱性的无色透明溶液中,不可能大量共存的是( )
A、Ca2+、Na+、NO
| ||||
B、K+、Ba2+、Cl-、NO
| ||||
C、HCO
| ||||
D、Ca2+、Cl-、K+、NO
|
下列各溶液中,微粒的物质的量浓度关系正确的是( )
| A、1.0 mol?L-1NH4Cl溶液:c(NH4+)=c(Cl-) |
| B、1.0 mol?L-1Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) |
| C、向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:c(Na+)=c(NO3-) |
| D、向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液 c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
在由水电离出的=1×10-14mol?L-1的溶液中,一定能大量共存的离子组是( )
| A、NH4+、Ba2+、NO3-、Cl- |
| B、Cl-、SO42-、Na+、K+ |
| C、SO42-、NO3-、Fe2+、Mg2+ |
| D、Na+、K+、ClO-、I- |
 某卡车上贴有如图标志,则它运输的化学品可能是 ( )
某卡车上贴有如图标志,则它运输的化学品可能是 ( )| A、液化气 | B、浓硫酸 |
| C、核废料 | D、食盐 |
下列各溶液中,粒子的物质的量浓度关系正确的是( )
| A、0.1mol?L-1氯化铵溶液中:c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| B、0.1mol?L-1的NaHCO3溶液中:c(Na+)+c(H+)=c(HCO3-)+c(OH-)+c(CO32-) |
| C、向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液中:c(OH-)>c(H+) |
| D、向硝酸钠溶液中滴加稀盐酸得到pH=5的混合溶液:c(Na+)=c(NO3-) |
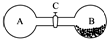 如图所示,容器A(容积2L)中有1×105 Pa的空气.在容器B(容积1L)中放入少量的只吸附氧气的吸附剂,保持真空.打开旋塞C,放置片刻,容器内的总压强变为0.6×105 Pa,这时气体中氮气和氧气的分子数之比最接近的数值是(吸附剂的体积可忽略不计)
如图所示,容器A(容积2L)中有1×105 Pa的空气.在容器B(容积1L)中放入少量的只吸附氧气的吸附剂,保持真空.打开旋塞C,放置片刻,容器内的总压强变为0.6×105 Pa,这时气体中氮气和氧气的分子数之比最接近的数值是(吸附剂的体积可忽略不计)( )
| A、8:1 | B、10:1 |
| C、12:1 | D、14:1 |
X、Y、Z、W是原子序数依次增大的短周期元素.X、W同主族,Z、W同周期,X原子核内质子数是Y原子核内质子数的
,W原子最外层电子数是Z原子最外层电子数的4倍.下列说法中正确的是( )
| 3 |
| 4 |
| A、原子半径:r(X)>r(Y)>r(W)>r(Z) |
| B、元素W的气态氢化物的热稳定性比元素X的强 |
| C、X、Y、Z三种元素形成的化合物中存在离子键和共价键 |
| D、Y和W形成的化合物的熔点肯定比Y和Z形成的化合物的熔点低 |