题目内容
铝是地壳中含量最高的金属元素,其单质及其合金在生产生活中的应用十分广泛.
(1)金属铝的生产是以Al2O3为原料,与冰晶石(Na3A1F6)在熔融状态下进行电解,其阴极电极反应式为 ,其电极均由石墨材料做成,则电解时不断消耗的电极是 (填“阴极”或“阳极”),冰晶石的作用为 .
(2)铝电池性能优越,A1-Ag2O电池可用作水下动力电源,化学反应为2Al+3Ag2O+2NaOH=2NaAl02+6Ag+H20,则负极的电极反应式为 ,正极附近溶液的pH (填“变大”“不变”或“变小”).
已知:①2Al(s)+3Cl2(g)═2AlCl3(s)△H1=-1390.8kJ/mol
②4Al(s)+3O2(g)═2Al2O3(s)△H2=-3339.6kJ/mol
③2C(s)+O2(g)═2CO(g)△H3=-221.0 kJ/mol
Al2O3(s)+3Cl2(g)+3C(s)═2AlCl3(s)+3CO(g)的△AH= .
(1)金属铝的生产是以Al2O3为原料,与冰晶石(Na3A1F6)在熔融状态下进行电解,其阴极电极反应式为
(2)铝电池性能优越,A1-Ag2O电池可用作水下动力电源,化学反应为2Al+3Ag2O+2NaOH=2NaAl02+6Ag+H20,则负极的电极反应式为
已知:①2Al(s)+3Cl2(g)═2AlCl3(s)△H1=-1390.8kJ/mol
②4Al(s)+3O2(g)═2Al2O3(s)△H2=-3339.6kJ/mol
③2C(s)+O2(g)═2CO(g)△H3=-221.0 kJ/mol
Al2O3(s)+3Cl2(g)+3C(s)═2AlCl3(s)+3CO(g)的△AH=
考点:电解原理,用盖斯定律进行有关反应热的计算
专题:
分析:(1)工业上采用电解Al2O3来制取Al,电解的阴极、阳极材料均由石墨材料做,因阳极上O2-失电子发生氧化反应生成O2,阴极铝离子得到电子发生还原反应生成铝,Al2O3的熔点很高,熔化得需要较多能量,加入助熔剂就可节约能量,降低熔化温度;
(2)依据电池反应分析元素化合价变化,负极是铝失电子在碱溶液中生成四羟基合铝酸钠,正极氧化银得到电子生成银依据碱性环境分析正极附近生成氢氧根离子;
依据盖斯定律将已知方程式变形并进行混合运算解答.
(2)依据电池反应分析元素化合价变化,负极是铝失电子在碱溶液中生成四羟基合铝酸钠,正极氧化银得到电子生成银依据碱性环境分析正极附近生成氢氧根离子;
依据盖斯定律将已知方程式变形并进行混合运算解答.
解答:
解:Ⅰ(1)用电解Al2O3来制取Al,电解的阴极、阳极材料均由石墨材料做,因阳极上O2-失电子发生氧化反应生成O2,阳极材料与该极上生成的O2反应被消耗,阴极铝离子得到电子发生还原反应生成铝,电极反应式为:Al3++3e-=Al,Al2O3的熔点很高,熔化得需要较多能量,加入助熔剂就可节约能量,降低熔化温度;
故答案为:Al3++3e-=Al;阳极; 降低氧化铝熔点;
(2)化学反应为2Al+3Ag2O+2NaOH+3H2O═2Na[Al(OH)4]+6Ag,负极是铝失电子在碱溶液中生成四羟基合铝酸钠,则负极的电极反应式:Al+4OH--3e-=[Al(OH)4-];正极氧化银得到电子生成银单质和氢氧根离子,所以正极溶液的pH变大;
①2Al(s)+3Cl2(g)═2AlCl3(s)△H1=-1390.8kJ/mol
②4Al(s)+3O2(g)═2Al2O3(s)△H2=-3339.6kJ/mol
③2C(s)+O2(g)═2CO(g)△H3=-221.0 kJ/mol
由盖斯定律知①-
+
得Al2O3(s)+3Cl2(g)+3C(s)═2AlCl3(s)+3CO(g),
△H=-1390.8kJ/mol-
×(-3339.6kJ/mol)+
×(-221.0 kJ/mol)=-52.5KJ/mol
故答案为:Al+4OH--3e-=AlO2-+2H2O;变大;-52.5KJ/mol.
故答案为:Al3++3e-=Al;阳极; 降低氧化铝熔点;
(2)化学反应为2Al+3Ag2O+2NaOH+3H2O═2Na[Al(OH)4]+6Ag,负极是铝失电子在碱溶液中生成四羟基合铝酸钠,则负极的电极反应式:Al+4OH--3e-=[Al(OH)4-];正极氧化银得到电子生成银单质和氢氧根离子,所以正极溶液的pH变大;
①2Al(s)+3Cl2(g)═2AlCl3(s)△H1=-1390.8kJ/mol
②4Al(s)+3O2(g)═2Al2O3(s)△H2=-3339.6kJ/mol
③2C(s)+O2(g)═2CO(g)△H3=-221.0 kJ/mol
由盖斯定律知①-
| ② |
| 2 |
| ③×3 |
| 2 |
△H=-1390.8kJ/mol-
| 1 |
| 2 |
| 3 |
| 2 |
故答案为:Al+4OH--3e-=AlO2-+2H2O;变大;-52.5KJ/mol.
点评:本题考查了电解原理、原电池工作原理,反应热的计算,侧重考查电极反应式的书写,掌握原电池、电解质的工作原理,明确电极反应式的书写原则,掌握盖斯定律求反应热的方法是解题关键,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法正确的是( )
| A、向2.0mL浓度均为0.lmol/L的KCl、KI混合溶液中滴加l~2滴0.01mol/LAgNO3溶液.振荡,沉淀呈黄色,说明AgCl的溶解度比AgI的溶解度小 |
| B、分别在Na2CO3和NaHCO3两种物质的溶液中,加入少量澄清石灰水,能用来鉴别这两种白色固体 |
| C、向0.1mol/L FeSO4溶液中滴加少量酸性KMnO4溶液,KMnO4溶液褪色,说明Fe2+具有氧化性 |
| D、向碘水中滴加CCl4,振荡静置后分层,CCl4层呈紫红色,说明可用CCl4从碘水中萃取碘 |
下列各组微粒中,核外电子总数相等的是( )
| A、H2O 和Al3+ |
| B、CO和CO2 |
| C、Na+和Li+ |
| D、NO和CO |
毕昇得了感冒,校医室的刘大夫给他打了青霉素,青霉素的俗名是( )
| A、头孢 | B、水杨酸 |
| C、阿司匹林 | D、盘尼西林 |
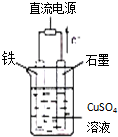 (1)已知298K时,1molC2H6在氧气中完全燃烧生成二氧化碳和液态水,利用该反应设计一个燃料电池:用氢氧化钾溶液做电解质溶液,用多孔石墨做电极,在电极上分别充入乙烷和氧气.写出负极的电极反应式
(1)已知298K时,1molC2H6在氧气中完全燃烧生成二氧化碳和液态水,利用该反应设计一个燃料电池:用氢氧化钾溶液做电解质溶液,用多孔石墨做电极,在电极上分别充入乙烷和氧气.写出负极的电极反应式