题目内容
15. 氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.
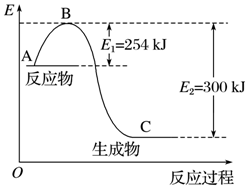
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用.(1)如图是N2(g)和H2(g)反应生成1mol NH3(g)过程中能量的变化示意图,请写出N2和H2反应的热化学方程式:N2(g)+3H2(g)=2NH3(g)△H=-92KJ/mol.
(2)若已知下列数据:
| 化学键 | H-H | N≡N |
| 键能/kJ•mol-1 | 435 | 943 |
(3)用NH3催化还原NOx还可以消除氮氧化物的污染.已知:
4NH3(g)+3O2(g)═2N2+6H2O(g)△H1=-a kJ•mol-1①
N2(g)+O2(g)═2NO(g)△H2=-b kJ•mol-1②
求:若1mol NH3还原NO至N2,则该反应过程中的反应热△H3=$\frac{3b-a}{4}$kJ•mol-1(用含a、b的式子表示).
(4)捕碳技术(主要指捕获CO2)在降低温室气体排放中具有重要的作用.目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下可逆反应:
反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)?(NH4)2CO3(aq)△H1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g)?NH4HCO3(aq)△H2
反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g)?2NH4HCO3(aq)△H3
请回答下列问题:
△H3与△H1、△H2之间的关系是△H3=2△H2-△H1.
分析 (1)据焓变等于反应物活化能减去生成物活化能求算焓变,再书写热化学方程式;
(2)据△H=反应物键能和-生成物键能和求算;
(3)已知①4NH3(g)+3O2(g)=2N2(g)+6H2O(g);△H1=-akJ/mol
②N2(g)+O2(g)=2NO(g);△H2=-bkJ/mol
利用盖斯定律将$\frac{①-3②}{4}$计算;
(4)根据盖斯定律,热化学方程式Ⅱ×2-热化学方程式Ⅰ可得热化学方程式Ⅲ,从而得出目标反应Ⅲ的焓变△H3.
解答 解:(1)据焓变等于反应物活化能减去生成物活化能求算焓变,N2和H2反应生成2mol NH3过程中的△H=(254KJ/mol-300KJ/mol)×2=-92KJ/mol,所以热化学方程式为N2(g)+3H2(g)=2NH3(g)△H=-92KJ/mol,故答案为:N2(g)+3H2(g)=2NH3(g)△H=-92KJ/mol;
(2)设N-H的键能为a,△H=反应物键能和-生成物键能和=943KJ/mol+3×435KJ/mol-6×aKJ/mol=-92KJ/mol,即a=390,故答案为:390;
(3)已知①4NH3(g)+3O2(g)=2N2(g)+6H2O(g);△H1=-akJ/mol
②N2(g)+O2(g)=2NO(g);△H2=-bkJ/mol
利用盖斯定律将$\frac{①-3②}{4}$可得NH3(g)+$\frac{3}{2}$NO(g)=$\frac{5}{4}$N2(g)+$\frac{3}{2}$H2O(g)△H3=$\frac{3b-a}{4}$kJ/mol,故答案为:$\frac{3b-a}{4}$;
(4)反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)═(NH4)2CO3(aq)△H1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g)═NH4HCO3(aq)△H2
根据盖斯定律Ⅱ×2-Ⅰ可得:(NH4)2CO3(aq)+H2O (l)+CO2(g)?2NH4HCO3(aq)△H3=2△H2-△H1,
故答案为:2△H2-△H1.
点评 本题考查了放热反应的图形分析、利用键能求算焓变以及盖斯定律在热化学方程式中的应用,题目难度中等,明确盖斯定律的含义及应用方法为解答关键,注意掌握热化学方程式的概念及书写原则,试题培养了学生灵活应用基础知识的能力.

 同步练习强化拓展系列答案
同步练习强化拓展系列答案| A. |  | B. |  | C. |  | D. |  |
| 主族 周期 | I A | II A | III A | IV A | V A | VI A | VII A | 0 |
| 2 | C | N | O | |||||
| 3 | Na | Mg | Si | S | Cl | Ar | ||
| 4 | Ca |
(2)S原子结构示意图为
 ;钙离子的电子式为:Ca2+.
;钙离子的电子式为:Ca2+.(3)第3周期元素中,最高价氧化物对应水化物酸性最强的是HClO4(填“H2SO4”或“HClO4”);
(4)C、N和O原子半径由小到大的顺序的是O<N<C;
(5)第3周期中气态氢化物最稳定的是HCl;(填“H2S”或“HCl”)
(6)Si是带来人类文明的重要元素之一,其氧化物化学式是SiO2;
(7)N元素形成的一种氢化物其水溶液呈碱性,请写出氢化物的化学式是NH3.
(8)铝是大自然赐予人类的宝物.它其中的一个用途是作为铝热剂,请写出铝和三氧化二铁发生反应的方程式2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.
 某温度下,Fe(OH)3(s)、Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化如图所示.据图分析,下列判断错误的是( )
某温度下,Fe(OH)3(s)、Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化如图所示.据图分析,下列判断错误的是( )| A. | Ksp[Fe(OH)3]<Ksp[Cu(OH)2] | |
| B. | Fe(OH)3、Cu(OH)2分别在b、c两点代表的溶液中达到饱和 | |
| C. | 加适量NH4Cl固体可使溶液由a点变到b点 | |
| D. | c、d两点代表的溶液中c(H+)与c(OH-)乘积相等 |
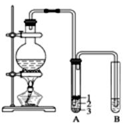 实验室制取少量溴乙烷的装置如图所示.根据题意完成下列填空:
实验室制取少量溴乙烷的装置如图所示.根据题意完成下列填空: