题目内容
10.氮族元素(Nitrogen group)是元素周期表VA 族的所有元素,包括氮(N)、磷(P)、砷(As)、锑(Sb)、铋(Bi)和Uup共计六种.(1)氮族元素的外围电子排布式的通式为ns2np3;基态磷原子中,电子占据的最高能层符号为M,该能层具有的原子轨道数为9.
(2)PH3分子的VSEPR模型为四面体形,键角NH3>H2O(填“>”、“<”或“=”).
(3)氮的最高价氧化物为无色晶体,它由两种离子构成:已知其阴离子构型为平面正三角形,则其阳离子中氮的杂化方式为sp杂化.
(4)从化合物NF3和NH3的结构与性质关系比较,回答它们两者如下性质差异原因:
①NF3的沸点为-129℃,而NH3的沸点为-33℃,其原因是NH3分子间存在较强的氢键,而NF3分子间仅有较弱的范德华力.
②NH3易与Cu2+反应,而NF3却不能,其原因是F的电负性大于N元素,NF3中N-F成键电子对偏向于F原子,N原子上的孤对电子难与铜离子形成配离子.
(5)磷化硼是一种受到高度关注的耐磨涂料,它可用作金属的表面保护层,磷化硼晶体的晶胞结构与金刚石类似,磷原子作面心立方最密堆积,则硼原子的配位数为4;已知磷化硼的晶胞边长a=478pm,计算晶体中硼原子和磷原子的核间距(dB-P)=207pm(保留三位有效数字).
分析 (1)氮族元素的外围电子为其最外层上s、p能级电子;基态磷原子中,电子占据的最高能层符号为M,该能层有1个s轨道、3个p轨道、5个d轨道;
(2)PH3分子中P原子价层电子对个数是4且含有一个孤电子对,根据价层电子对互斥理论判断该分子的VSEPR模型,成键电子对和孤电子对之间的排斥力小于孤电子对之间的排斥力,据此判断键角;
(3)氮的最高价氧化物为N2O5,由两种离子构成,其中阴离子构型为平面正三角形,化学式应为NO3-,则其阳离子的化学式为:NO2+,其中心原子价电子对数为 2+$\frac{5-1-2×2}{2}$=2,根据价层电子对互斥理论判断原子杂化方式;
(4)①分子晶体中含有氢键的物质熔沸点较高;
②NF3中N-F成键电子对偏向于F原子,N原子上的孤对电子难与铜离子形成配离子;
(5)磷化硼结构如图所示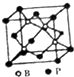 ,该晶胞中B原子为4个、P原子个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,每个B原子连接4个P原子,则硼原子的配位数为4;晶体中硼原子和磷原子的核间距(dB-P)等该晶胞体对角线的 $\frac{1}{4}$,据此计算.
,该晶胞中B原子为4个、P原子个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,每个B原子连接4个P原子,则硼原子的配位数为4;晶体中硼原子和磷原子的核间距(dB-P)等该晶胞体对角线的 $\frac{1}{4}$,据此计算.
解答 解:(1)氮族元素的外围电子为其最外层上s、p能级电子,则氮族元素外围电子排布式为ns2np3;基态磷原子中,电子占据的最高能层符号为M,该能层有1个s轨道、3个p轨道、5个d轨道,所以有9个轨道,
故答案为:ns2np3;M;9;
(2)PH3分子中P原子价层电子对个数是4且含有一个孤电子对,根据价层电子对互斥理论判断该分子的VSEPR模型为四面体形,成键电子对和孤电子对之间的排斥力小于孤电子对之间的排斥力,氨气分子中只含一个孤电子对、水分子中含有两个孤电子对,所以键角,
故答案为:四面体形;>;
(3)氮的最高价氧化物为N2O5,由两种离子构成,其中阴离子构型为平面正三角形,化学式应为NO3-,则其阳离子的化学式为:NO2+,其中心原子价电子对数为2+$\frac{5-1-2×2}{2}$=2,根据价层电子对互斥理论判断原子杂化方式为sp,
故答案为:sp杂化;
(4)①NH3存在氢键,而NF3只存在分子间作用力,两种作用力前者较强,物质的沸点较高,
故答案为:NH3分子间存在较强的氢键,而NF3分子间仅有较弱的范德华力;
②F的电负性大于N元素,NF3中N-F成键电子对偏向于F原子,N原子上的孤对电子难与铜离子形成配离子,所以NF3不易与Cu2+形成配离子,
故答案为:F的电负性大于N元素,NF3中N-F成键电子对偏向于F原子,N原子上的孤对电子难与铜离子形成配离子;
(5)磷化硼结构如图所示 ,该晶胞中B原子为4个、P原子个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,每个B原子连接4个P原子,则硼原子的配位数为4;已知磷化硼的晶胞边长a=478pm,则晶胞的体对角线长为$\sqrt{3}$a,晶体中硼原子和磷原子的核间距应为体对角线的$\frac{1}{4}$,所以dB-P=$\frac{1}{4}$$\sqrt{3}$×478pm=207pm,
,该晶胞中B原子为4个、P原子个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,每个B原子连接4个P原子,则硼原子的配位数为4;已知磷化硼的晶胞边长a=478pm,则晶胞的体对角线长为$\sqrt{3}$a,晶体中硼原子和磷原子的核间距应为体对角线的$\frac{1}{4}$,所以dB-P=$\frac{1}{4}$$\sqrt{3}$×478pm=207pm,
故答案为:4;207.
点评 本题考查物质结构和性质,为高频考点,涉及晶胞计算、氢键、键角、微粒空间构型、原子核外电子排布等知识点,侧重考查学生知识应用、计算、空间想象能力,难点是晶胞计算,注意该晶胞中B-P原子核间距,题目难度中等.

 阅读快车系列答案
阅读快车系列答案| A. | 硅的化学性质稳定,常温下不与任何物质反应 | |
| B. | 硅是构成矿物和岩石的主要元素,硅元素在地壳中的含量居第一位 | |
| C. | 硅在自然界中可以以游离态存在 | |
| D. | 高纯度的单质硅被广泛用于制作计算机芯片 |
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得.
①基态Ti原子的外围电子排布图为
 ,电子占据的最高能层具有的原子轨道数为16.
,电子占据的最高能层具有的原子轨道数为16.②LiBH4由Li+和BH4-构成.BH4-的立体结构是正四面体,B原子的杂化轨道类型是sp3,
BH4-内部含有的微粒间作用力有cd(a.离子键b.非极性键c.极性键d.配位键e.氢键).
Li、B、H元素的电负性由大到小排列顺序为H>B>Li.
(2)金属氢化物是具有良好发展前景的储氢材料.
①LiH中,离子半径Li+<H-(填“>”、“=”或“<”).
②某储氢材料是第三周期金属元素M的氢化物.M的部分电离能如表所示:
| I1/kJ•mol-1 | I2/kJ•mol-1 | I3/kJ•mol-1 | I4/kJ•mol-1 | I5/kJ•mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
(3)NaH具有NaCl型晶体结构,已知NaH晶体的晶胞参数a=488pm(棱长),Na+半径为102pm,
H-的半径为142pm,NaH的理论密度是$\frac{24×4}{{N}_{A}×48{8}^{3}×1{0}^{-30}}$g•cm-3
(只列算式,不必计算出数值,阿伏加德罗常数为NA)
| A. | 3 mol/(L•s) | B. | 2mol/(L•s) | C. | 1.5 mol/(L•s) | D. | 0.5mol/(L•s) |
| A. | 同一原子中,2p、3p、4p能级的轨道数依次增多 | |
| B. | 电子排布式(22Ti)1s22s22p63s23p10违反了能量最低原则 | |
| C. |  表示的原子能量处于最低状态 表示的原子能量处于最低状态 | |
| D. | 正三价阳离子的电子排布式为1s22s22p63s23p63d5的元素在周期表中位于Ⅷ族 |
| 元素 | 相关信息 |
| X | 其一种同位素,可被用作相对原子质量的标准 |
| Y | 其最高价氧化物对应水化物能与其气态氢化物相互间发生化合反应 |
| P | 是短周期中(除稀有气体外)原子半径最大的元素 |
| Q | 存在质量数为25,中子数为13的核素 |
| W | 位于周期表第13列 |
| R | 与Z同族,且最高价氧化物对应水化物的浓溶液常温下与W单质会出现钝化现象 |
(2)T的单质易溶于XT4中,理由是:Cl2、CCl4均为非极性分子,相似相溶.
(3)根据下表中信息,判断下列化合物固态的晶体类型(填“离子晶体”…等):
| 化合物 | X3Y4 | R2T2 |
| 晶体类型 | ||
| 熔点/℃ | >3600 | -76 |
(5)在25℃、101kPa下,已知13.5g的W固体单质在Z2气体中完全燃烧后恢复至原状态,放热419kJ,写出表示W单质燃烧热的热化学方程式Al(s)+$\frac{3}{2}$O2(g)=$\frac{1}{2}$Al2O3(s)△H=-838kJ/mol.
(6)化合物P2R溶液在空气中长期放置,与氧气反应会生成与过氧化钠的结构相似的物质P2R2,其溶液显黄色,则P2R2的电子式为
 ,用化学方程式表示P2R溶液在空气中的变质过程4Na2S+O2+2H2O═4NaOH+2Na2S2.
,用化学方程式表示P2R溶液在空气中的变质过程4Na2S+O2+2H2O═4NaOH+2Na2S2. 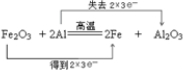 .
.


