题目内容
17.下列各组中的反应,属于同一反应类型的是( )| A. | 由溴乙烷制乙醇;由乙烯与水反应制乙醇 | |
| B. | 乙烯使溴的CCl4溶液褪色;甲苯使酸性高锰酸钾溶液褪色 | |
| C. | 由苯制硝基苯;由环己醇制环己烯 | |
| D. | 由乙酸和乙醇制乙酸乙酯;苯与液溴在FeBr3催化下制溴苯 |
分析 A.由溴乙烷制乙醇,-Br转化为-OH;由乙烯与水反应制乙醇,碳碳双键转化为单键;
B.乙烯使溴的CCl4溶液褪色,碳碳双键转化为单键;甲苯使酸性高锰酸钾溶液褪色,甲基转化为-COOH;
C.由苯制硝基苯,苯环上H被硝基取代;由环己醇制环己烯,-OH转化为碳碳双键;
D.由乙酸和乙醇制乙酸乙酯,为酯化反应;苯与液溴在FeBr3催化下制溴苯,苯中H被Br取代.
解答 解:A.由溴乙烷制乙醇,-Br转化为-OH,为水解反应;由乙烯与水反应制乙醇,碳碳双键转化为单键,为加成反应,故A不选;
B.乙烯使溴的CCl4溶液褪色,碳碳双键转化为单键,为加成反应;甲苯使酸性高锰酸钾溶液褪色,甲基转化为-COOH,为氧化反应,故B不选;
C.由苯制硝基苯,苯环上H被硝基取代,为取代反应;由环己醇制环己烯,-OH转化为碳碳双键,为消去反应,故C不选;
D.由乙酸和乙醇制乙酸乙酯,为酯化反应;苯与液溴在FeBr3催化下制溴苯,苯中H被Br取代,均为取代反应,故D选;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机反应为解答的关键,侧重分析与应用能力的考查,注意有机反应的判断,题目难度不大.

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目
18.洋蓟属高档蔬菜,从洋蓟提取的物质A具有良好的保健功能和药用价值,A在酸性条 件下水解可生成B和C,反应可表示为
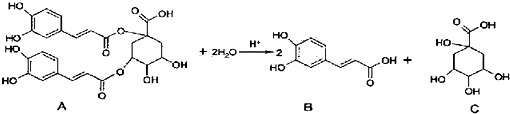
下列说法正确的是( )

下列说法正确的是( )
| A. | B中共面的原子个数最多为20个 | |
| B. | 1mol A 和足量NaOH 溶液反应,最多消耗11molNaOH | |
| C. | B 能和浓溴水发生反应,1mol B最多消耗4 molBr2 | |
| D. | A、C分子中手性碳原子个数相同 |
19.下列关于阿佛加德罗常数(NA)的说法中不正确的是( )
| A. | 1 mol N4分子的质量是56 g | |
| B. | 标况下,NA个 H2O分子含有3NA个原子 | |
| C. | 常温下,1 mo/L 的NH4Cl 溶液中NH4+的浓度小于1 mol/L | |
| D. | 高温高压,催化剂条件下,28 g N2分子与6 g H2充分反应可生成34 g NH3 |
12.下列电子式中,书写正确的是( )
| A. | 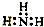 | B. | 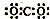 | C. | 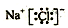 | D. | 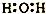 |
9.关于由锌、铜和稀硫酸构成的原电池的下列说法中正确的是( )
| A. | 锌是负极,铜是正极 | B. | 电子从铜片经导线流向锌片 | ||
| C. | 负极的反应式为2H++2e-=H2 | D. | 反应一段时间后,溶液的酸性增强 |
6.玻璃、水泥、陶瓷属于( )
| A. | 金属材料 | B. | 无机非金属材料 | C. | 有机高分子材料 |
7.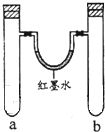 某化学小组用以下装置做兴趣实验(试管中有空气存在).
某化学小组用以下装置做兴趣实验(试管中有空气存在).
(1)实验1,同时加入试剂,反应开始可观察到U形管中液面b(填编号),简述产生该现象的原因钠与水反应比钠与乙醇反应快,所以开始时a试管中产生的氢气比b试管多,故液面应左低右高.
a.左高右低b.左低右高c.左右相平d.来回震荡
(2)写出钠与乙醇反应的化学方程式2CH3CH2OH+2Na→2CH3CH2ONa+H2↑;反应结束静置一段时间,最终U形管中液面c(填题(1)编号).
(3)实验2,U形管中液面a(填题(1)编号);写出a试管中发生还原反应的电极反应方程式O2+2H2O+4e→4OH-.
(4)实验3,U形管中液面左低右高,检验b管中生成新物质的操作是取样,加入KSCN溶液,溶液变红,说明有Fe3+生成.
(5)其他条件不变情况下,将实验4a、b试管中硝酸同时改为3mLcd(填编号),即可观察到U形管液面产生相反现象.
a.无水乙醇b.浓硫酸c.稀硫酸d.浓盐酸
(6)常温下,在a、b试管中分别加入等体积的同种溶液,仅对a试管进行强光照射,一段时间后观察到U型管液面左低右高,根据所学知识,推测该溶液为氯水(写名称).
 某化学小组用以下装置做兴趣实验(试管中有空气存在).
某化学小组用以下装置做兴趣实验(试管中有空气存在).| 实验编号 | a中试剂 | b中试剂 |
| 1 | 0.1克Na、3mL水 | 0.1克Na、3mL乙醇 |
| 2 | 铁钉、3mL饱和食盐水 | 铁钉、3mL饱和氯化铵 |
| 3 | 3mL水 | 3mL饱和FeSO4溶液 |
| 4 | 3mL浓硝酸、1g铝片 | 3mL浓硝酸、1g铜片 |
a.左高右低b.左低右高c.左右相平d.来回震荡
(2)写出钠与乙醇反应的化学方程式2CH3CH2OH+2Na→2CH3CH2ONa+H2↑;反应结束静置一段时间,最终U形管中液面c(填题(1)编号).
(3)实验2,U形管中液面a(填题(1)编号);写出a试管中发生还原反应的电极反应方程式O2+2H2O+4e→4OH-.
(4)实验3,U形管中液面左低右高,检验b管中生成新物质的操作是取样,加入KSCN溶液,溶液变红,说明有Fe3+生成.
(5)其他条件不变情况下,将实验4a、b试管中硝酸同时改为3mLcd(填编号),即可观察到U形管液面产生相反现象.
a.无水乙醇b.浓硫酸c.稀硫酸d.浓盐酸
(6)常温下,在a、b试管中分别加入等体积的同种溶液,仅对a试管进行强光照射,一段时间后观察到U型管液面左低右高,根据所学知识,推测该溶液为氯水(写名称).