题目内容
15.甲、乙两种粒子都只含有一个原子核,且核内具有相同数目的质子,这两种微粒一定是( )| A. | 同种原子 | B. | 同种元素 | ||
| C. | 互为同位素 | D. | 具有相同的核外电子排布 |
分析 根据原子核的构成进行分析解答,原子核是由质子和中子构成的,甲、乙两种粒子都只含有一个原子核,且核内具有相同数目的质子,质子数相同的单原子为同种元素.
解答 解:A.甲、乙两种粒子都只含有一个原子核,且核内具有相同数目的质子,可能为不同种原子,如$\underset{\stackrel{1}{\;}}{1}\underset{\stackrel{\;}{H}}{\;}\underset{\stackrel{\;}{\;}}{\;}$、$\underset{\stackrel{2}{\;}}{1}\underset{\stackrel{\;}{H}}{\;}$,故A错误;
B.元素是具有相同核内质子数的一类原子的总称,甲、乙两种粒子都只含有一个原子核,且核内具有相同数目的质子,为同种元素,故B正确;
C.同位素是质子数相同,而中子数不同的原子,甲、乙两种粒子都只含有一个原子核,且核内具有相同数目的质子,不一定都是原子,可能为原子和离子,如H+、H,故C错误;
D.甲、乙两种粒子都只含有一个原子核,且核内具有相同数目的质子,不一定具有相同的核外电子排布,如钠原子的核外电子排布可以表示为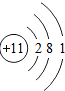 ,钠离子的核外电子排布可以表示为
,钠离子的核外电子排布可以表示为 ;钠离子的核外电子排布为2、8,硫离子核外电子排布为2、8、8,不相同,故D错误;
;钠离子的核外电子排布为2、8,硫离子核外电子排布为2、8、8,不相同,故D错误;
故选B.
点评 本题考查原子的构成,注意相关概念的理解和把握,题目难度不大,为易错题,可用枚举法解答.

练习册系列答案
相关题目
6.只用一种试剂,可区别Na2SO4、NH4Cl、MgSO4四种溶液,这种试剂是( )
| A. | HCl | B. | BaCl2 | C. | AgNO3 | D. | NaOH |
3.下列化学方程式或离子方程式正确的是( )
| A. | 过量的NaOH与Ca(HCO3)2反应:2OH-+Ca2++2HCO3-═CaCO3↓+2H2O+CO32- | |
| B. | 苯酚钠溶液中通入少量二氧化碳:C6H5O-+CO2+H2O→C6H5OH+HCO3- | |
| C. | 乙酸乙酯与氢氧化钠溶液反应:CH3COOC2H5+OH-→CH3COOH+C2H5O- | |
| D. | 向含有Fe2O3悬浊液中通入HI:Fe2O3+6H+=2Fe3++3H2O |
10.高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂.下列反应可制取K2FeO4:
2Fe(OH)3+3Cl2+10KOH$\frac{\underline{\;0-30℃\;}}{\;}$2K2FeO4+6KCl+8H2O,
对于该反应,下列说法正确的是( )
2Fe(OH)3+3Cl2+10KOH$\frac{\underline{\;0-30℃\;}}{\;}$2K2FeO4+6KCl+8H2O,
对于该反应,下列说法正确的是( )
| A. | 该反应是置换反应 | |
| B. | Cl2是氧化剂 | |
| C. | Fe(OH)3发生还原反应 | |
| D. | 每生成1mol K2FeO4转移电子的物质的量为3mol |
7.下列说法中用离子方程式表达正确的是( )
| A. | 氯气溶于水:Cl2+H2O?H++Cl-+HClO | |
| B. | 向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O=2A1 (OH)3↓+CO32- | |
| C. | Fe(NO3)2溶液中滴加少量稀盐酸:Fe2++NO3-+4H+=Fe3++NO↑+2H2O | |
| D. | 用醋酸溶液除去水垢:2H++CaCO3=Ca2++CO2↑+H2O |
4.实验室制取氯化氢,有关叙述正确的是( )
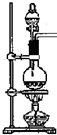

| A. | 利用浓硫酸的吸水性和氧化性 | |
| B. | 开始制备气体时应先加热后向烧瓶中加硫酸 | |
| C. | 利用浓硫酸的难挥发性和酸性 | |
| D. | 组装完实验装置立即加试剂、加热制气体 |
5.实验室用锌片与2mol/L硫酸溶液制取氢气,下列措施不能使反应速率加快的是( )
| A. | 加热 | |
| B. | 滴加少量的CuSO4溶液 | |
| C. | 不用稀硫酸,改用更多的18mol/L硫酸溶液 | |
| D. | 不用铁片,改用铁粉 |