题目内容
下表列出了断裂某些化学键所需要的能量: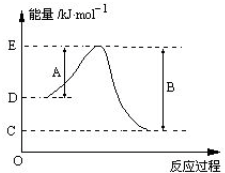
请回答下列问题:
(1)如图表示某反应的能量变化关系图,此反应为 (填“放热”或“吸热”)反应,其中△H= (用含A或B的字母表示)kJ mol-1.
(2)若此能量变化关系图表示反应:H2(g)+1/2O2(g)=H2O(g)△H=-241.8kJ mol-1,则B= kJ mol-1,X=
(3)表示Cl2与HI气体反应生成碘蒸气与氯化氢的热化学方程式
(4)请写出满足下列要求的热化学方程式:
①反应物中化学键的断裂和生成物中化学键的形成均在上表中.
②此反应不是置换反应,也不是化合反应.
③化学方程式中所有物质的相对分子质量都不大于80.
④反应前后分子总数不变.

| 化学键 | H-H | Cl-Cl | I-I | O=O | C-Cl | C-H | O-H | H-Cl | H-I |
| kJ/mol | 436 | 247 | 151 | X | 330 | 413 | 463 | 431 | 299 |
(1)如图表示某反应的能量变化关系图,此反应为
(2)若此能量变化关系图表示反应:H2(g)+1/2O2(g)=H2O(g)△H=-241.8kJ mol-1,则B=
(3)表示Cl2与HI气体反应生成碘蒸气与氯化氢的热化学方程式
(4)请写出满足下列要求的热化学方程式:
①反应物中化学键的断裂和生成物中化学键的形成均在上表中.
②此反应不是置换反应,也不是化合反应.
③化学方程式中所有物质的相对分子质量都不大于80.
④反应前后分子总数不变.
考点:热化学方程式
专题:化学反应中的能量变化
分析:(1)从反应物和生成物能量大小分析;△H=-(反应物总能量-生成物总能量);
(2)△H=反应物键能和-生成物键能和,键能和等于其活化能;
(3)先据△H=反应物键能和-生成物键能和求出反应的△H,再书写热化学方程式;
(4)根据反应的条件结合化学键键能来计算焓变.
(2)△H=反应物键能和-生成物键能和,键能和等于其活化能;
(3)先据△H=反应物键能和-生成物键能和求出反应的△H,再书写热化学方程式;
(4)根据反应的条件结合化学键键能来计算焓变.
解答:
解:(1)反应物能量高于生成物,正反应放热;△H=-(反应物总能量-生成物总能量)=-(D-C)kJ/mol=(C-D)kJ/mol,
故答案为:放热;C-D;
(2)B表示1mol水的键能,为2×463kJ/mol=926kJ/mol;△H=反应物键能和-生成物键能和=436kJ/mol+
xkJ/mol-2×463kJ/mol=-241.8kJ/mol,x=496.4kJ/mol,
故答案为:926;496.4;
(3)热化学方程式为:Cl2(g)+2HI(g)=2HCl(g)+I2(g)△H=反应物键能和-生成物键能和=247kJ/mol+(299kJ/mol×2)-(431kJ/mol×2)-151kJ/mol=-168kJ/mol,
故答案为:Cl2(g)+2HI(g)=I2(g)+2HCl(g)△H=-168kJ/mol.
(4)符合条件的化学方程式为:Cl2(g)+CH4(g)=CH3Cl(g)+HCl(g),此时△H=-[(413×3+330+431)-(247+413×4)]kJ/mol=
=-101kJ/mol,故答案为:Cl2(g)+CH4(g)=CH3Cl(g)+HCl(g)△H=-101kJ/mol.
故答案为:放热;C-D;
(2)B表示1mol水的键能,为2×463kJ/mol=926kJ/mol;△H=反应物键能和-生成物键能和=436kJ/mol+
| 1 |
| 2 |
故答案为:926;496.4;
(3)热化学方程式为:Cl2(g)+2HI(g)=2HCl(g)+I2(g)△H=反应物键能和-生成物键能和=247kJ/mol+(299kJ/mol×2)-(431kJ/mol×2)-151kJ/mol=-168kJ/mol,
故答案为:Cl2(g)+2HI(g)=I2(g)+2HCl(g)△H=-168kJ/mol.
(4)符合条件的化学方程式为:Cl2(g)+CH4(g)=CH3Cl(g)+HCl(g),此时△H=-[(413×3+330+431)-(247+413×4)]kJ/mol=
=-101kJ/mol,故答案为:Cl2(g)+CH4(g)=CH3Cl(g)+HCl(g)△H=-101kJ/mol.
点评:本题考查了△H=反应物键能和-生成物键能和以及热化学方程式书写,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
关于电解氯化钠溶液,下列叙述正确的是 ( )
| A、原电池的正极和电解池的阴极所发生的反应类型相同 |
| B、若在阳极附近的溶液中滴入KI淀粉试液,溶液呈蓝色 |
| C、若在阴极附近的溶液中滴入酚酞试液,溶液仍无色 |
| D、电解一段时间后,将全部电解液转移到烧杯中,加入适量盐酸充分搅拌后溶液可恢复原状况 |
下列物质中,属于酸性氧化物但不溶于水的是( )
| A、CO2 |
| B、SiO2 |
| C、SO2 |
| D、Fe2O3 |
某种兴奋剂的结构简式如图,有关该物质的叙述中,正确的是( )


| A、遇氯化铁溶液显色 |
| B、能和NaHCO3反应产生CO2 |
| C、1 mol该物质分别能和4 mol溴、7 mol氢气完全反应 |
| D、滴入酸性高锰酸钾溶液,紫色褪去,证明结构中存在碳碳双键 |
2012-09-25安徽省机动车氮氧化物总量减排现场会召开,会议指出,要积极推进机动车污染防治.为了减轻大气污染,科学家正在研究利用催化技术将汽车尾气中的NO和CO转变成CO2和N2,即2NO+2CO?2CO2+N2△H<0若反应在恒容的密闭容器中进行,下列有关说法正确的是( )
| A、单位时间内消耗CO和CO2.的物质的量相等时,反应达到平衡状态 |
| B、平衡时,其他条件不变,升高温度可提高CO的转化率 |
| C、使用高效催化剂,提高正反应速率、降低逆反应速率 |
| D、平衡前,随着反应的进行,容器内压强始终不变 |
设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A、100mL0.1mol/L K2SO4 溶液中,含有氧原子数为0.04NA |
| B、100g 17%的氨水中,含有氨分子的数为NA |
| C、1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,转移的电子数NA |
| D、25℃时,1.0L pH=13的Ba(OH)2溶液中,含有0.2NA OH- |
糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质,以下叙述正确的是( )
| A、植物通过光合作用将CO2转化成葡萄糖是太阳能转变成热能的过程 |
| B、油脂属于酯类化合物,油脂的水解反应叫皂化反应 |
| C、淀粉与纤维素互称为同分异构体 |
| D、浓硝酸溅在皮肤上,使皮肤呈黄色是由于浓硝酸和蛋白质发生了颜色反应 |


