题目内容
8.图是298K 时N2与H2反应过程中能量变化的曲线图.下列叙述正确的是( )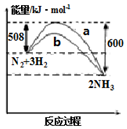
| A. | 该反应的热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=92kJ•mol-1 | |
| B. | b曲线是升高温度时的能量变化曲线 | |
| C. | 加入催化剂,该化学反应的活化能和反应热都改变 | |
| D. | 在温度体积一定的条件下,通入lmol N2和3molH2 反应后放出的热量为Q1kJ,若通入2mol N2和6mol H2 反应后放出的热量为Q2kJ,则184>Q2>2Q1 |
分析 A.由图可知,反应物的总能量大于生成物的总能量,焓变等于正逆反应活化能之差;
B.b为使用催化剂,降低反应的活化能,而焓变不变;
C.催化剂降低反应的活化能;
D.物质的量与热量成正比,热化学方程式中为完全转化的能量变化,但合成氨为气体体积减小的可逆反应,压强增大平衡正向移动.
解答 解:A.由图可知,反应物的总能量大于生成物的总能量,焓变等于正逆反应活化能之差,则N2(g)+3H2(g)?2NH3(g)△H=-92kJ•mol-1,故A错误;
B.图中反应的活化能降低,而焓变不变,则b曲线是使用催化剂时的能量变化曲线,故B错误;
C.催化剂降低反应的活化能,而焓变不变,故C错误;
D.物质的量与热量成正比,热化学方程式中为完全转化的能量变化,但合成氨为气体体积减小的可逆反应,压强增大平衡正向移动,则通入lmol N2和3molH2 反应后放出的热量为Q1kJ,若通入2mol N2和6mol H2 反应后放出的热量为Q2kJ,则184>Q2>2Q1,故D正确;
故选D.
点评 本题考查反应热与焓变,为高频考点,把握图中能量变化、催化剂对活化能的影响、平衡移动为解答的关键,侧重分析与应用能力的考查,注意选项D为解答的难点,题目难度不大.

练习册系列答案
相关题目
3.在标准状况下,将6.72LH2S和6.72LO2混合引燃,待反应完全后,恢复至标况下,把气体通入到NaOH溶液中,得到盐的质量是( )
| A. | 25.2g | B. | 18.9g | C. | 23.4g | D. | 48.6g |
20.下列说法正确的是( )
| A. | 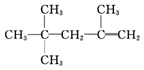 的名称为2,2,4-三甲基-4-戊烯 的名称为2,2,4-三甲基-4-戊烯 | |
| B. | 化合物 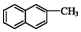 不是苯的同系物 不是苯的同系物 | |
| C. | 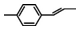 分子中所有碳原子一定共平面 分子中所有碳原子一定共平面 | |
| D. | 除甲酸外的羧酸均不能使高锰酸钾酸性溶液褪色 |
17.下列各组物质,前者属于电解质,后者属于非电解质的是( )
| A. | NaCl晶体、BaSO4 | B. | 铜、二氧化硫 | ||
| C. | 熔融的KNO3、酒精 | D. | 液态的醋酸、硫酸溶液 |
 .C与氢元素可分别形成含10个电子的分子、阴离子和阳离子,阳离子中中心原子的杂化类型为sp3
.C与氢元素可分别形成含10个电子的分子、阴离子和阳离子,阳离子中中心原子的杂化类型为sp3