题目内容
按照不同的分类标准,H2SO4、NaOH、HCl、CH3COOH四种物质中,有一种与另外三种有明显的不同,请写出这种物质的化学式及分类的依据(写出两种):
(1)这种物质是 ,分类依据是 .
(2)这种物质是 ,分类依据是 .
(1)这种物质是
(2)这种物质是
考点:酸、碱、盐、氧化物的概念及其相互联系
专题:物质的分类专题
分析:(1)根据物质的酸碱性判断;
(2)根据物质的组成元素分析.
(2)根据物质的组成元素分析.
解答:
解:(1)H2SO4、NaOH、HCl、CH3COOH四种物质中,NaOH为碱性物质,其它的为酸性物质,所以根据物质的酸碱性分类;
故答案为:NaOH;物质的酸碱性;
(2)H2SO4、NaOH、HCl、CH3COOH四种物质中,HCl中不含氧元素,其它三种都含有氧元素;
故答案为:HCl;组成中是否含氧.
故答案为:NaOH;物质的酸碱性;
(2)H2SO4、NaOH、HCl、CH3COOH四种物质中,HCl中不含氧元素,其它三种都含有氧元素;
故答案为:HCl;组成中是否含氧.
点评:本题考查了物质的分类,解答时要分析物质的元素组成和物质的性质,题目难度不大.

练习册系列答案
相关题目
在A、B、C三试管中分别盛有Cl-、Br-、I- 的溶液,向A试管中加入新制的氯水和CCl4,出现分层,下层为橙红色,再将此溶液倒入C试管中,无变化,则A、B、C三支试管中所盛有的离子依次是( )
| A、I-、Br-、Cl- |
| B、Br-、I-、Cl- |
| C、Cl-、I-、Br- |
| D、Br-、Cl-、I- |
如图是立方烷的球棍模型,下列有关说法不正确的是( )
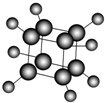

| A、其一氯代物只有一种 |
| B、其二氯代物有三种 |
| C、分子中σ键均由sp3-s电子云重叠而成 |
| D、它与苯乙烯(C6H5-CH=CH2)互为同分异构体 |
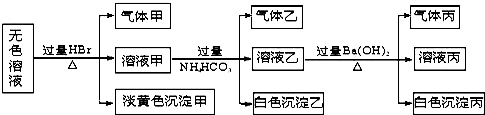
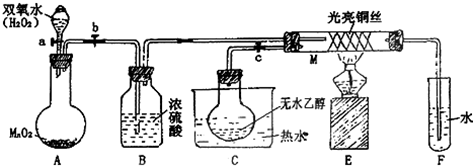
 Ⅰ.施莱辛(Schlesinger)等人提出可用NaBH4与水反应制氢气:BH4-+2H2O═BO2-+4H2↑(反应实质为水电离出来的H+被还原).研究表明,该反应生成H2的速率受外界条件影响.下表为pH和温度对NaBH4半衰期的影响(半衰期是指反应过程中,某物质的浓度降低到初始浓度一半时所需的时间).
Ⅰ.施莱辛(Schlesinger)等人提出可用NaBH4与水反应制氢气:BH4-+2H2O═BO2-+4H2↑(反应实质为水电离出来的H+被还原).研究表明,该反应生成H2的速率受外界条件影响.下表为pH和温度对NaBH4半衰期的影响(半衰期是指反应过程中,某物质的浓度降低到初始浓度一半时所需的时间).