题目内容
12.已知甲、乙、丙、X是四种中学化学中常见的物质,其转化关系如图所示.则甲和X不可能是( )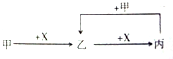
| A. | 甲为C,X为O2 | B. | 甲为Fe,X为Cl2 | ||
| C. | 甲为CO2,X为NaOH溶液 | D. | 甲为HCl,X为Na2CO3溶液 |
分析 A.甲为C、X为O2,则乙为CO,丙为CO2;
B.甲为Fe、X为Cl2,乙为FeCl3,氯化铁不能与氯气反应
C.甲为CO2、X为NaOH,乙为NaHCO3,丙为Na2CO3;
D.甲为HCl,X为Na2CO3溶液,乙为CO2,丙为NaHCO3.
解答 解:A.甲为C,X是O2,则乙为CO,丙为CO2,丙(CO2)和甲(C)反应又可以生成乙(CO),所以符合转化关系,故A不选;
B.甲为Fe、X为Cl2,乙为FeCl3,不能发生乙、丙的相互转化,故B选;
C.甲为CO2、X为NaOH,乙为NaHCO3,丙为Na2CO3,丙(Na2CO3)和甲(CO2)、H2O又可以生成乙(NaHCO3),符合转化关系,故C不选;
D.甲为HCl,X为Na2CO3溶液,乙为CO2,丙为NaHCO3,碳酸氢钠与盐酸反应可以得到二氧化碳,符合转化关系,故D不选.
故选B.
点评 本题考查无机物的推断,属于验证型题目,侧重于物质性质的考查,题目难度不大.

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
15.在一定条件下,将PCl3(g)和Cl2(g)充入体积不变的2L密闭容器中发生下述反应:PCl3(g)+Cl2(g)?PCl5(g);5min末达到平衡,有关数据如表.
下列判断不正确的是( )
| PCl3(g) | Cl2(g) | PCl5(g) | |
| 初始浓度(mol•L-1) | 2.0 | 1.0 | 0 |
| 平衡浓度(mol•L-1) | c1 | c2 | 0.4 |
| A. | 若升高温度,反应的平衡常数减小,则正反应为吸热反应 | |
| B. | 反应5 min内,v(PCl3)=0.08 mol•L-1•min-1 | |
| C. | 当容器中为1.2 mol Cl2时,可逆反应达到平衡状态 | |
| D. | 平衡后移走2.0 mol PCl3和1.0 mol Cl2,在相同条件下再达平衡时,c(PCl5)<0.2 mol/L |
3.在一定条件下,反应A2(g)+B2(g)═2AB(g) 达到平衡状态的是( )
| A. | 单位时间内生成n mol的AB的同时,生成n mol的A2 | |
| B. | 单位时间内生成n mol A2的同时,生成n mol的B2 | |
| C. | 容器内的总压强不随时间而变化 | |
| D. | 单位时间内生成2n mol AB的同时,生成n mol的B2 |
20.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 在标准状况下,11.2LCI2含有的分子数为NA | |
| B. | 32gO2中所含有的氧原子数为NA | |
| C. | 2.4g镁变成镁离子,转移的电子数为0.2NA | |
| D. | 1L0.3mol/LK2SO4溶液中含有的K+数为0.3NA |
17.下列说法正确的是( )
| A. | 纤维素和淀粉遇碘水均呈蓝色 | |
| B. | 油脂可用来制造肥皂 | |
| C. | 石油分馏得到的汽油是纯净物 | |
| D. | 煤的气化属于物理变化,煤的干馏属于化学变化 |
4.下列有关实验的操作、原理和现象,正确的是( )
| A. | 比较去锈的铁钉和去锈的绕有细铜丝的铁钉与同浓度的盐酸反应速率快慢时,可以加K3[Fe(CN)4]溶液,观察铁钉周围出现蓝色沉淀的快慢 | |
| B. | 受强酸或强碱腐蚀致伤时,应先用大量水冲洗,再用2%醋酸溶液饱和硼酸溶液洗,最后用水冲洗,并视情况作进一步处理 | |
| C. | 实验室用已知浓度的酯酸溶液滴定未知浓度的氢氧化钠溶液时,选用酚酞做指示剂比用甲基橙做指示剂时带来的误差要大一点 | |
| D. | 自来水厂常用某些含铝或铁的化合物作净水剂,是由于它们具有杀菌作用 |
1.为了除去FeSO4溶液中的Fe3+,可用加入纯铁屑,但此法很费时;现有一种方法是在蒸馏水沸腾时加入粉未状的绿矾(少量多次),搅拌,直到观察到有褐色沉淀产生即可停止加入药品,煮沸1~2分钟,趁热过滤,密封保存所得的FeSO4溶液,此法的原理是( )
| A. | Fe3+易水解,它的水解产物之一能抑制的Fe2+水解 | |
| B. | Fe2+有较强的还原性,它能还原Fe3+ | |
| C. | Fe3+有较强的氧化性,它能氧化Fe2+ | |
| D. | Fe3+的水解是吸热反应,升温能促进它的水解 |
 .
.