题目内容
20.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )| A. | 在标准状况下,11.2LCI2含有的分子数为NA | |
| B. | 32gO2中所含有的氧原子数为NA | |
| C. | 2.4g镁变成镁离子,转移的电子数为0.2NA | |
| D. | 1L0.3mol/LK2SO4溶液中含有的K+数为0.3NA |
分析 A.依据N=$\frac{V}{22.4}$×NA计算;
B.质量转化为物质的量结合1个氧气分子含有2个氧原子解答;
C.镁为2价金属,2.4g镁的物质的量为0.1mol,0.1mol镁完全反应失去0.2mol电子;
D.根据n=cV计算硫酸钾的物质的量,每摩尔硫酸钾含有2mol钾离子,再根据N=nNA计算离子的数目.
解答 解:A.在标准状况下,11.2LCI2含有的分子数=$\frac{V}{22.4}$×NA=$\frac{11.2L}{22.4L/mol}$×NA=0.5NA,故A错误;
B.32gO2中所含有的氧原子数=$\frac{32g}{32g/mol}$×2×NA=2NA,故B错误;
C.镁为2价金属,2.4g镁的物质的量为0.1mol,0.1mol镁完全反应失去0.2mol电子,转移的电子数为0.2NA,故C正确;
D.1L溶液中含有K+离子数为1L×0.3mol/L×2×NA=0.6NA,故D错误;
故选:C.
点评 本题考查阿伏加德罗常数的有关计算和判断,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系是解题关键,题目难度不大.

练习册系列答案
相关题目
3.2008年北京奥运会的“祥云”火炬所用燃料的主要成分是丙烷,下列有关丙烷的叙述中,不正确的是( )
| A. | 分子中碳原子不在一条直线上 | B. | 光照不能够发生取代反应 | ||
| C. | 是石油分馏的一种产品 | D. | 比丁烷更易液化 |
11.现有几组物质的熔点数据如下表:
据此回答下列问题:
(1)A组属于原子晶体晶体,其熔化时克服的微粒间的作用力是共价键;
(2)B组晶体共同的物理性质是①②③④(填序号);①有金属光泽 ②导电性 ③导热性 ④延展性
(3)C组中HF熔点反常是由于HF分子间存在氢键;
(4)D组晶体可能具有的性质是②④(填序号);①硬度小 ②水溶液能导电 ③固体能导电 ④熔融状态能导电.
| A组 | B组 | C组 | D组 |
| 金刚石:3110℃ | Li:181℃ | HF:-83℃ | NaCl:801℃ |
| 硅晶体:1410℃ | Na:98℃ | HCl:-114℃ | KCl:776℃ |
| 硼晶体:2300℃ | K:64℃ | HBr:-89℃ | RbCl:718℃ |
| 二氧化硅:1723℃ | Rb:39℃ | HI:-51℃ | CsCl:645℃ |
(1)A组属于原子晶体晶体,其熔化时克服的微粒间的作用力是共价键;
(2)B组晶体共同的物理性质是①②③④(填序号);①有金属光泽 ②导电性 ③导热性 ④延展性
(3)C组中HF熔点反常是由于HF分子间存在氢键;
(4)D组晶体可能具有的性质是②④(填序号);①硬度小 ②水溶液能导电 ③固体能导电 ④熔融状态能导电.
12.已知甲、乙、丙、X是四种中学化学中常见的物质,其转化关系如图所示.则甲和X不可能是( )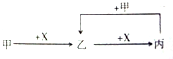

| A. | 甲为C,X为O2 | B. | 甲为Fe,X为Cl2 | ||
| C. | 甲为CO2,X为NaOH溶液 | D. | 甲为HCl,X为Na2CO3溶液 |
9.金丝桃素的结构简式如图所示,下列有关它的说法正确的是( )


| A. | 属于芳香烃 | B. | 分子中苯环上的一氯代物有3种 | ||
| C. | 不能与金属钠发生反应 | D. | 不能发生水解反应 |
10.离子液体(Ionic Iiquid),是指由有机阳离子和阴离子构成的在室温下呈液态的盐类化合物,具有蒸汽压低、熔点低、液程宽、易操作、可溶性好和稳定性高等特征,正逐步应用于科技和社会生活领域.一种合成“离子液体”的原料咪唑: ,分子式:C3H4N2,与苯有类似结构和性质.有关它的说法错误的是( )
,分子式:C3H4N2,与苯有类似结构和性质.有关它的说法错误的是( )
 ,分子式:C3H4N2,与苯有类似结构和性质.有关它的说法错误的是( )
,分子式:C3H4N2,与苯有类似结构和性质.有关它的说法错误的是( )| A. | 是芳香族化合物 | |
| B. | 能发生加成、取代、氧化反应 | |
| C. | 每个分子中有9个σ键 | |
| D. | 分子极性键又含有非极性键中既含有 |
 ,
,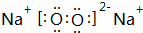 .若用球棍模型表示①和④形成的化合物的分子结构,应该是下图中的B.
.若用球棍模型表示①和④形成的化合物的分子结构,应该是下图中的B.
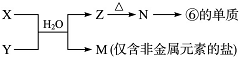
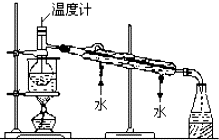 海洋植物如海带中含有丰富的碘元素,碘元素以碘离子的形式存在.某研究性学习小组设计如下实验从海带中提取碘,请你完成下面相关问题:
海洋植物如海带中含有丰富的碘元素,碘元素以碘离子的形式存在.某研究性学习小组设计如下实验从海带中提取碘,请你完成下面相关问题: