题目内容
A、B、C、D、E、F六种短周期元素的原子序数依次增大.已知A原子的最外层电子数是次外层电子数的3倍,B、C、F三原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均能生成盐和水,D元素原子的最外层电子数比次外层电子数少4个,E元素原子的最外层电子数是内层电子数的一半.试回答:
(1)写出下列元素的符号D ,E .
(2)B原子的结构示意图 ,A离子的结构示意图 .
(3)F 在周期表中的位置 ;
(4)F单质与水反应的离子方程式
(5)B、D两种元素最高价氧化物的水化物之间反应的离子方程式 .
(1)写出下列元素的符号D
(2)B原子的结构示意图
(3)F 在周期表中的位置
(4)F单质与水反应的离子方程式
(5)B、D两种元素最高价氧化物的水化物之间反应的离子方程式
考点:位置结构性质的相互关系应用
专题:
分析:A原子的最外层电子数是次外层电子数的3倍,最外层最多8个电子,则A最外层含有6个电子,为O元素;B、C、F三原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均能生成盐和水,则C为Al元素,则B为Na、F为Cl元素;D元素原子的最外层电子数比次外层电子数少4个,则D最外层含有4个电子,为ⅣA族元素,则D为Si元素;E元素原子的最外层电子数是内层电子数的一半,E的原子序数大于Si,则E的能层电子数为10,最外层含有5个电子,则E为P元素,据此进行解答.
解答:
解:A原子的最外层电子数是次外层电子数的3倍,最外层最多8个电子,则A最外层含有6个电子,为O元素;B、C、F三原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均能生成盐和水,则C为Al元素,则B为Na、F为Cl元素;D元素原子的最外层电子数比次外层电子数少4个,则D最外层含有4个电子,为ⅣA族元素,则D为Si元素;E元素原子的最外层电子数是内层电子数的一半,E的原子序数大于Si,则E的能层电子数为10,最外层含有5个电子,则E为P元素,
(1)根据分析可知,D为Si元素、E为P元素,
故答案为:Si;P;
(2)B为Na元素,钠的原子序数为11,最外层含有1个电子,钠原子结构示意图为: ;A为氧离子,氧离子的核电荷数为8,核外电子总数为10,氧离子结构示意图为:
;A为氧离子,氧离子的核电荷数为8,核外电子总数为10,氧离子结构示意图为: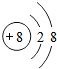 ,
,
故答案为: ;
;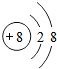 ;
;
(3)F为Cl元素,其核外电子层数为3,最外层含有7个电子,氯原子在周期表中的位置为:第三周期ⅤⅡA族,
故答案为:第三周期ⅤⅡA族;
(4)F为氯元素,其单质为氯气,氯气和水反应生成盐酸和次氯酸,次氯酸是弱酸,反应的离子方程式:Cl2+H2O=H++Cl-+HClO;
故答案为:Cl2+H2O=H++Cl-+HClO;
(5)B为Na元素、D为Si元素,二者的最高价氧化物对应的水化物分别为NaOH和H2SiO3,二者反应的离子方程式为:2OH-+H2SiO3=SiO32-+2H2O,
故答案为:2OH-+H2SiO3=SiO32-+2H2O.
(1)根据分析可知,D为Si元素、E为P元素,
故答案为:Si;P;
(2)B为Na元素,钠的原子序数为11,最外层含有1个电子,钠原子结构示意图为:
 ;A为氧离子,氧离子的核电荷数为8,核外电子总数为10,氧离子结构示意图为:
;A为氧离子,氧离子的核电荷数为8,核外电子总数为10,氧离子结构示意图为: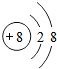 ,
,故答案为:
 ;
;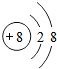 ;
;(3)F为Cl元素,其核外电子层数为3,最外层含有7个电子,氯原子在周期表中的位置为:第三周期ⅤⅡA族,
故答案为:第三周期ⅤⅡA族;
(4)F为氯元素,其单质为氯气,氯气和水反应生成盐酸和次氯酸,次氯酸是弱酸,反应的离子方程式:Cl2+H2O=H++Cl-+HClO;
故答案为:Cl2+H2O=H++Cl-+HClO;
(5)B为Na元素、D为Si元素,二者的最高价氧化物对应的水化物分别为NaOH和H2SiO3,二者反应的离子方程式为:2OH-+H2SiO3=SiO32-+2H2O,
故答案为:2OH-+H2SiO3=SiO32-+2H2O.
点评:本题考查了位置、结构与性质关系的应用,题目难度中等,正确推断各元素名称为解答关键,注意掌握原子结构与元素周期律、元素周期表的关系,试题培养了学生灵活应用基础知识的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在使用下列各实验装置时,不合理的是( )
A、 装置用于分离CCl4和H2O的混合物 |
B、 装置用于收集H2、CO2、Cl2等气体 |
C、 装置用于吸收NH3或HCl,并防止倒吸 |
D、 装置用于收集NH3,并吸收多余的NH3 |
 常温下,取一定量的PbI2固体配成饱和溶液,T时刻改变某一条件,离子的浓度变化如图所示,(注:第一次平衡时c(I-)=2×10-3mol/L,c(Pb2+)=2×10-3mol/L)下列有关说法正确的是( )
常温下,取一定量的PbI2固体配成饱和溶液,T时刻改变某一条件,离子的浓度变化如图所示,(注:第一次平衡时c(I-)=2×10-3mol/L,c(Pb2+)=2×10-3mol/L)下列有关说法正确的是( )| A、常温下,Ksp=2×10-6 |
| B、温度不变,向PbI2饱和溶液中加入少量硝酸铅浓溶液,PbI2的溶解度不变,c(Pb2+)不变 |
| C、T时刻改变的条件是升高温度,PbI2的,Ksp 增大 |
| D、常温下Ksp[PbS]=8×10-28,向PbI2的悬浊液中加入Na2S溶液,PbI2(s)+S2-(aq)?PbS(s)+2I-(aq)反应的化学平衡常数为5×1018 |
下列化学实验事实及其解释都正确的是( )
| A、向碘水中滴加CCl4,振荡静置后分层,CCl4层呈紫红色,说明可用CCl4从碘水中萃取碘 |
| B、向SO2水溶液中滴加盐酸酸化的Ba(NO3)2溶液,有白色沉淀生成,说明BaSO3难溶于盐酸 |
| C、向0.1mol?L-1FeSO4溶液中滴加少量酸性KMnO4溶液,KMnO4溶液褪色,说明Fe2+具有氧化性 |
| D、向2.0mL浓度均为0.1mol?L-1的KCl、KI混合溶液中滴加1~2滴0.01mol?L-1 AgNO3溶液,振荡,沉淀呈黄色,说明同温度下AgCl的Ksp比AgI的Ksp 大 |
下列说法正确的是( )
| A、放电影有一条光束,说明空气是一种胶体,故空气带电 |
| B、铁闸连接铜片,可防止被海水腐蚀 |
| C、硫酸亚铁铵晶体过滤后,用无水乙醇替代水洗涤,可减少晶体损失 |
D、聚合物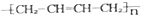 的单体为CH3-CH=CH-CH3 的单体为CH3-CH=CH-CH3 |
 在3支试管中分别放有:①1mL苯和3mL水;②1mL溴苯和3mL水;③1mL乙醇和3mL水.图中三支试管从左到右的排列顺序为( )
在3支试管中分别放有:①1mL苯和3mL水;②1mL溴苯和3mL水;③1mL乙醇和3mL水.图中三支试管从左到右的排列顺序为( )| A、①②③ | B、①③② |
| C、②①③ | D、②③① |
下列反应中不需加热的吸热反应是( )
| A、锌粒与稀硫酸的反应 |
| B、灼热的木炭与CO2反应 |
| C、甲烷在氧气中的燃烧反应 |
| D、Ba(OH)2?8H2O晶体与NH4Cl晶体的反应 |


 是食品添加剂的增香原料,其香味比香草醛更浓郁.写出乙基
是食品添加剂的增香原料,其香味比香草醛更浓郁.写出乙基
 )是一种医药中间体,请设计合理方案用茴香醛(
)是一种医药中间体,请设计合理方案用茴香醛( )合成D.(其他原料自选,用反应流程图表示并注明必要的反应条件).
)合成D.(其他原料自选,用反应流程图表示并注明必要的反应条件).